Erste Schritte
"Basislabor" (oft Haus-spezifisches Standardprofil) inkludiert meist:
- Kleines Blutbild
- Klinische Chemie (Natrium, Kalium, Harnstoff, Kreatinin, CRP, TSH, Glukose)
- Gerinnung (INR, PTT)
- BGA (venös, inkl. Elektrolyte + Glukose)
Ergänzung je nach klinischem Verdacht und Leitsymptom
(z.B. großes Blutbild, "Leber- / Bauchwerte" (ALT, AST, GGT, AP, Bilirubin, Lipase), Troponin, D-Dimere, LDH, CK, TSH, fT3/ft4, PCT... etc.)
Tipps
Bei auffälligen Laborwerten immer hinterfragen: Ist der Wert plausibel?
→ Führend ist immer die Klinik von Patient:innen, nicht ein einzelner Laborwert!
Einzelne seltene, aber potentiell kritische Erkankungen präsentieren sich evtl. auch durch „typische“ Laborkonstellationen.
Neben laborchemischen Fehlern gibt es eine Vielzahl von Fehlerquellen im schnellen Alltag einer Notaufnahme, z.B.:
- Falsche Patient:in (insb. bei unplausiblen Werten oder auffälligen Änderungen zu Vor-Laborwerten)
- Abnahme am Infusionsarm (typisch bei kristalloider Infusionslösung: Anämie, Elektrolytstörungen)
- Langes Stauen oder „Stochern“, forcierte Aspiration durch kleine Nadel, Aspiration von Hämatom: Hämolyse → (falsche) Hyperkaliämie
- Falsches Behandeln der Probe:
- Zu starkes Schütteln: Hämolyse (etwas Schwenken ist allerdings gut)
- Nicht ausreichend gefülltes Röhrchen (v.a. bei Gerinnung): Fehlerhafte Werte
- Lange liegen lassen (insb. bei BGA-Röhrchen): Hämolyse, Hypoxie, sonstige Fehler
GuruFacts
BGA
BGA - Abnahmeort und Informationen
Abnahmeort:
- venöse BGA (bei spO2 >95% zur initialen Evaluierung meist ausreichend)
- eine relevante respiratorische Azidose zeigt sich auch in der venösen BGA
- arterielle BGA (besser zur Beurteilung der respiratorischen Situation geeignet, insb. Oxygenierung)
- kapilläre BGA (weniger Schmerzen bei Entnahme - aber korrekte Abnahme bei Zentralisation kaum möglich, geeignet für Kleinkinder oder stabile Pat.)
Informationen:
- Säure/Base Status (pH, Bikarbonat, Base Exzess)
- respiratorische Situation (pO2, pCO2)
- Metabolik (Elektrolyte, Laktat)
- Zusatzinformationen je nach System (Hämoglobin, metHb, COHb etc.)
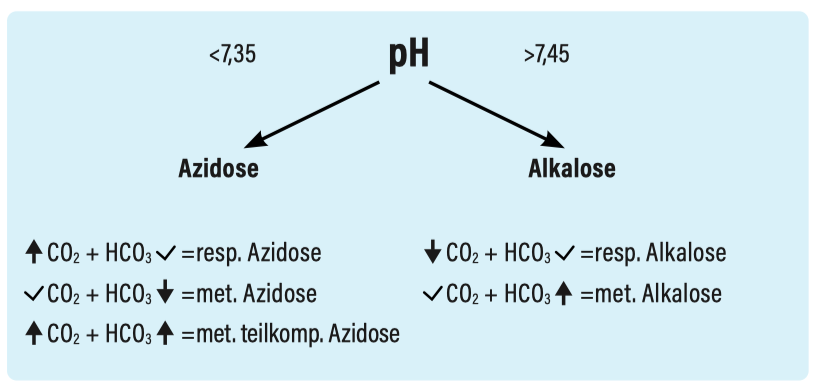
Basis-Interpretation
(vereinfachtes Schema)
Normalwerte BGA
BGA Normalwerte
Messwert | Normal | Kommentar |
|---|---|---|
paO2 | 65–100 mmHg | nur in art./kap. Abnahme verwertbar Korrektur bei Hyperventilation (Schätzwert): PaO2(korr) = PaO2(ist) - 1,6 x (40-PaCO2(ist)) |
saO2 | 95-99% | |
pCO2 (art) | 32–45 mmHg | |
pCO2 (ven) | 45-50 mmHg | |
Base Excess (BE) | -2 bis +2 | |
Bicarbonat (HCO3) | 22-26 mmol/l |
Azidose
Azidose - Ursachen
Respiratorische Azidose:
- COPD/Asthma? (ggf. NIV erwägen!)
- Hypoventilation (Opiat, Beatmungseinstellung?)
Metabolische Azidose:
- Laktatazidose
- Hinweis: Ringer-Laktat löst keine Laktatazidose aus (und verschlimmert diese nicht)
- Ketoazidose (Diabetes, Hyperglykämie, SGLT2-Inhibitoren)
- Niereninsuffizienz
Bicarbonat niedrig! (ggf. Dialyse notwendig?) - Anionenlücke vergößert?
Azidose - Auswirkungen
- Rechtsverschiebung der Sauerstoffbindungskurve (O2 wird besser ins Gewebe abgegeben)
- Gerinnungsaktivität eingeschränkt
- zerebrale Vasodilatation (Hirndruck)
- Insbes. bei metabolischer Azidose: „Pseudohyperkaliämie“ durch Kaliumshift aus den Zellen ins Plasma (grobe Formel: -0,1 pH=ca. +0,4-0,6mmol/l Kalium)
- Bei diabetischer Ketoazidose ist Hyperkaliömie a.e. nicht durch Shift, sondern durch absoluten Insulinmangel erklärt.
- Ausnahmen: Kaliumdepletion durch (vorherigen) z.B. gastrointestinalen Verlust, hier auch Hypokaliämie möglich
Checkliste Azidose
- Respiratorische Azidose nicht puffern sondern beatmen!
- Metabolische Azidose:
- Immer Anionenlücke berechnen (s. unten): Intoxikation?
- Falls Intubation nötig: Mit hohem Minutenvolumen beatmen! Angestrebtes CO2 zur Kompensation einer metabolische Azidose: pCO2= (1,5x aktuelles HCO3) + 8 (s. auch "physiologisch schwieriger Atemweg")
- Kalium oft falsch hoch, daher bei erfolgreicher Therapie engmaschige Kontrolle, frühzeitige Kaliumsubstitution)
Alkalose
Alkalose - Ursachen
Respiratorische Alkalose:
- Hyperventilation
(ggf. zum Ausgleich einer Hypoxie? Lungenembolie? Sepsis?)
Metabolische Alkalose:
- Salzsäureverlust (z.B. massives Erbrechen)
- Diuretikaeinnahme (Subtraktions- bzw. Kontraktionsalkalose)
- Bicarbonat-Zufuhr (z.B. bei Kalium-Brausetabletten etc.)
Alkalose - Auswirkungen
- Linksverschiebung der Sauerstoffbindungskurve (O2 wird schlechter ins Gewebe abgegeben)
- Kalzium wird verstärkt an Albumin gebunden, daher Dysästhesie und Tetanie insb. in den Akren (wie) bei Hyperventilation
- zerebrale Vasokonstriktion (kurzfristige Senkung Hirndruck)
Checkliste Alkalose
- CAVE: Hyperventilation / Tachypnoe immer ernst nehmen! (ev. handelt es sich um die versuchte Kompensation einer metabolischen Azidose (z.B. diab. Ketoazidose) oder Folge von Lungenembolie, Pneumonie, etc.)
- Keine weitere Basenzufuhr (keine Brausetabletten)
- Eine metabolische Alkalose kann nur sehr beschränkt respiratorisch kompensiert werden
Kombinierte Säure-Base-Störungen
Kombinierte Säure-Base-Störungen + Kompensationen
Erwartete Kompensation nach "Boston-Modell":
Bei möglichen kombinierten Störungen (z.B. gleichzeitig vorliegende respiratorische Azidose und metabolische Alkalose) hilft die Einschätzung der erwarteten Veränderung der anderen Parameter. Verändern sich die Parameter im erwarteten Ausmaß oder liegt eine zweite, parallele oder gegenläufige bzw. überlappende Störung vor? Wichtig zur Beurteilung ist auch die Klinik und Anamnese, insb. die Schnelligkeit der Entwicklung.
In diesem Modell: Normalwerte für CO2 40mmHg; HCO3 24mmol/l
Respiratorische Azidose:
- Akut: Pro 10mmgH ↑CO2 (>40mmHg) erwartet 1mmol/l ↑HCO3
- Chronisch: Pro 10mmHg CO2 (>40mmHg) erwartet 3,5mmol/l ↑HCO3
Respiratorische Alkalose:
- Akut: Pro 10mmgH ↓CO2 (<40mmHg) erwartet 2mmol/l ↓HCO3
- Chronisch: Pro 10mmgH ↓CO2 (<40mmHg) erwartet 4mmol/l ↓HCO3
Metabolische Störungen:
- Metabolische Azidose: Pro 1mmol/l ↓HCO3 erwartet 1,2mmHg ↓CO2
- Metabolische Alkalose: Pro 1mmol/l ↑HCO3 erwartet 0,7mmHg ↑CO2
Anionenlücke
Formel: Natrium - (HCO 3 + Chlorid)
Normalwert: 3-11mmol/l
Bei jeder metabolischen Azidose berechnen!
Anionenlücke - Grafik
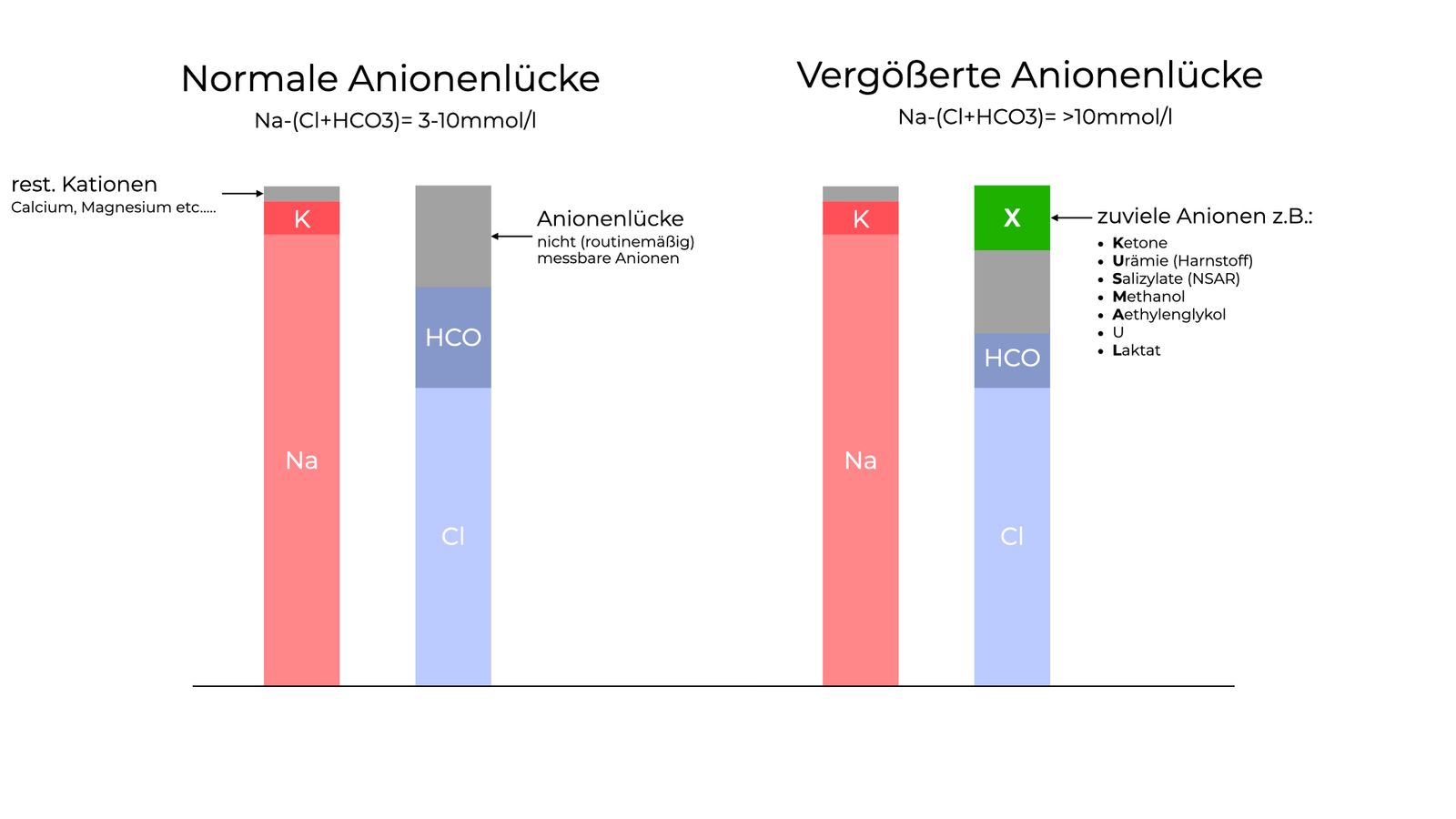
Die Anionenlücke grafisch in grau dargestellt. Links eine normale Anionenlücke, rechts eine vergrößerte Anionenlücke – vergrößert, weil ein unbekanntes Anion zusätzlich vorliegt.
Checkliste vergrößter Anionenlücke
- Nierenfunktionseinschränkung? (Harnstoff normal?)
- Diabetes / Hyperglykämie
- Diabetische Ketoazidose (Hyperglykämie + Ketone im Urin/Blut?
- Bei SGLT2-Inhibitor-Einnahme: Erwäge euglykäme Ketoazidose)
- Diabetische Ketoazidose (Hyperglykämie + Ketone im Urin/Blut?
- Laktat erhöht? (z.B. Schock, Leberinsuffizienz, Thiaminmangel, Metformin)
- Alle “nein”? → hochgradiger Verdacht auf Intoxikation!
- Bei auffälliger Anamnese z.B. Suizidversuch, unklares Koma, "komisches Bauchgefühl" bei vergrößerten Anionenlücke immer aktiv nach Intoxikationen suchen!
Sonderfall: Verkleinerte (ggf. sogar negative) Anionenlücke - Ursachen
selten!
- Hypalbuminämie (Leberschaden?)
- Lithiumintoxikation
- Hyperchloridämie
Ketone
Urämie
Salizylate (ASS/NSAR)
Methanol
Aethylenglykol (z.B. Frostschutzmittel)
Urämie (2.)
Laktat
Elektrolyte
Kalium - Hypokaliämie
Hypokaliämie - Symptomatik
- Oft diffuse Symptomatik, u.a.
- (Muskel)Schwäche bis zu Rhabdomyolyse
- Obstipation bis zu Ileus
- Arrhythmien
- Hochrisiko-Patient:innen: Ältere Pat., kardiale Vorerkrankungen, Antiarrhythmika
- EKG: Vermehrte Extrasystolen, flache Ts
Je schneller Hypokaliämie eintritt, desto ausgeprägter ist meist die Symptomatik.
CAVE: Bei schwerer Hyperglykämie und niedrig/grenzwertigem Kaliumspiegel (etwa <3,3mmol/l): Rascher K-Abfall bei Insulin-Gabe möglich! Frühzeitig Kalium-Substitution iv.
- 3-3,5mmol/l: Leichte Hypokaliämie (oft asymptomatisch)
→ orale Substitution - <3mmol/l: Moderat-schwere Hypokaliämie
- ab <2,5mmol/l bedrohlich
Hypokaliämie - häufige Ursachen
- Kaliumverlust:
- Intestinal z.B. Diarrhö, Laxantieneinnahme
- Renal z.B. Diuretika, Nierenerkrankungen wie Nephritiden, polyurisches Nierenversagen; Hyperaldosteronismus; Glukokortikoidtherapie
- „Shift“ in Zellen:
- Insulin
- Alkalose
- Hypothermie
- Adrenalin-Gabe
- Verminderte Kaliumzufuhr (meist nur geringe Hypokaliämie)
Checkliste Hypokaliämie <2,5-3mmol/l
- EKG-Monitoring!
- Ziel: Kalium >3mmol/l
- Auslöser therapieren (s. oben)
- Intravenöse Substitution (z.B. 40mmol KCl pro 1.000ml VEL)
- max. 20mmol/h (= 1.000ml+40mmol KCl über 2h) in gut laufendem Zugang, bei längerer Gabe ZVK + Kalium-Perfusor
- Bei Lebensbedrohung durch Hypokaliämie bis 40mmol/h - Risikoabwägung!
- bereits ab 10mmol/h Venenreizung beschrieben. Bei Schmerzen an Infusionsort: Infusionsgeschwindigkeit reduzieren
- CAVE: Infusion mit Kalium deutlich markieren, peripher niemals "pur" verabreichen!
- Magnesiumspiegel kontrollieren, bei Hypomagnesiämie: Magnesiumsulfat 10% 10-20ml über 1h iv. (ca. 4-8mmol Mg); je nach Spiegel ggf. wiederholen
Kalium - Hyperkaliämie
Häufige Fehlerquelle: Hämolyse bei Blutentnahme (z.B. langes Stauen, hoher Druck bei Entnahme, geschüttelte Proben) = (falsche) Hyperkaliämie.
Hauptrisiko: Rhythmusstörungen
Reanimation bei V.a. ursächliche Hyperkaliämie, siehe Reanimation
Insb. bei terminaler Niereninsuffizienz + Hyperkaliämie frühzeitig Kontakt mit Dialyse-Team. Bei Dialyse-Pat. oft unterschiedliche Toleranz erhöhter Kalium-Spiegel.
- >5-5,9mmol/l: milde Hyperkaliämie
→ Therapie nach Volumenstatus + Auslöser - >6,0mmol/l: moderat-schwere Hyperkaliämie
→ oft relevante Symptomatik, Notfalltherapie! - Dialysepat. + Hyperkaliämie
→ Rücksprache Dialyse! Oft chronisch erhöhtes Kalium.
Hyperkaliämie - häufige Ursachen
- Vermehrte Kalium-Zufuhr
meist in Kombination mit Niereninsuffizienz- Kalium-Präparate
- Kaliumreiche Nahrungsmittel (z.B. Bananen)
- Niereninsuffizienz (akut/chronisch)
- Medikamentös
- Kaliumsparende Diuretika
- ACE-Hemmer, Sartane
- „Shift“ aus den Zellen
- (massive) Hyperglykämie
- Azidose
- Kaliumfreisetzung
u.a. bei Rhabdomyolyse, Tumorlyse, Hämolyse
(in aufsteigender Reihenfolge bei zunehmender Hyperkaliämie):EKG-Zeichen bei Hyperkaliämie
(„Bei bizarrem EKG, denke an Kalium!“)
Checkliste Hyperkaliämie >6,0mmol/l
= moderat-schwere Hyperkaliämie
- Bei EKG-Veränderungen (insb. QRS-Verbreiterung, Bradykardie):
- Zellmembranstabilisierung: Calciumgluconat 10% 30ml (6,8mmol Ca) KI iv. (eingeschränkte Evidenz)
- Dialyse (insb. bei EKG-Veränderungen raschestmöglich)
- Medikamentöse Therapie - "Kalium-Shift"
(falls keine Akut-Dialyse / zur Überbrückung. CAVE: Nach ca. 3-4h wieder Kalium-Shift “zurück”, daher engmaschige Verlaufskontrolle):- Insulin-Glukose: Insulin 10IE + Glucose 25g
(Details siehe Tabelle unten, Wirkeintritt nach ca. 15-30 min.)- Stündliche BZ-Kontrollen (Glukose wirkt ca. 1h; Insulin 2-3h)
- Betamimetika: Salbutamol 10-20mg inhal. (CAVE: 1 Amp. oft „nur“ 1,25mg, 1 DA-Hub meist nur 0,1mg!)
- Natriumbikarbonat bei Azidose: NaBic 8,4% 50-100ml iv. KI (eingeschränkte Evidenz)
- Erwäge zusätzlich Kalium-Binder
- Insulin-Glukose: Insulin 10IE + Glucose 25g
Kalium-Binder (Details und Dosierungen)
Kaliumelimination mittels Kaliumbinder (Patiromer oder Natrium-Zirkonium-Zyklosilikat = SZC) insb. bei Niereninsuffizienz erwägen
- Wirkeintritt erst nach mehreren Stunden = keine alleinigen Notfallmedikamente!
- Multiple Wechselwirkungen und Nebenwirkungen beachten (z.B. QT-Verlängerung, GI-Beschwerden, Bindung von anderen Medikamenten), bisher eingeschränkte Evidenz
- Natrium-Zirkonium-Zyklosilikat (z.B. Lokelma®): 10g /8h po. für 24-72h oder
- Patiromer 8,4g/24h po.
- Routinemäßge Nutzung von Polystyrolsulfonat (z.B. Resonium®) in der Akuttherapie wird zunehmend kritisch beurteilt
Hyperkaliämie: Insulin + Glukose Infusion
Insulin-Glukose bei Hyperkaliämie
Blutzucker-Spiegel | Insulin Dosis | + Glukose Dosis |
|---|---|---|
<100mg/dl | 5-10IE* | 50g = G40% 120ml (ad Infusion) |
100-200mg/dl | 10IE* | 25g = G40% 60ml (ad Infusion) |
>200mg/dl | 10IE | keine |
*Bei erhöhtem Risiko für Hypoglykämie (BZ <150mg/dl (8,33mmol/l), Niereninsuffizienz, kein bekannter Diabetes Mellitus, <60kg Körpergewicht, ♀︎): Reduktion auf 5 IE Insulin erwägen. Alternativ/additiv: Glukose-Infusion (G10% mit 50ml/h über 5h (insg. 250ml = 25g)
Checkliste Hyperkaliämie >5-5,9mmol/l ohne EKG-Veränderungen
Bei Instabilitätszeichen Therapie wie bei schwerer Hyperkaliämie!
- Therapie nach Volumenstatus
- Bei Hypervolämie: Diuretikagabe (z.B. Furosemid 40mg iv. bei Diuretika-Naivität; Dosierung Diuretika um ca. 50% erhöhen bei bestehender Diuretika-Therapie)
- Bei Hypovolämie: Volumengabe (Vollelektrolytlösung nach Bedarf, bei Azidose ggf. isotone NaBic-Lösung (425ml G5% + 75ml NaBic 8,4%)
- Auslöser beenden/beheben
- Medikamente absetzen/pausieren wenn möglich, insb. ACE-Hemmer, AT1-Hemmer (Sartane), Spironolacton
- Ursache behandeln, z.B. relevante Hyperglykämie, akute Niereninsuffizienz
- Erwäge Kalium-Binder
Kalium-Binder (Details und Dosierungen)
Kaliumelimination mittels Kaliumbinder (Patiromer oder Natrium-Zirkonium-Zyklosilikat = SZC) insb. bei Niereninsuffizienz erwägen
- Wirkeintritt erst nach mehreren Stunden = keine alleinigen Notfallmedikamente!
- Multiple Wechselwirkungen und Nebenwirkungen beachten (z.B. QT-Verlängerung, GI-Beschwerden, Bindung von anderen Medikamenten), bisher eingeschränkte Evidenz
- Natrium-Zirkonium-Zyklosilikat (z.B. Lokelma®): 10g /8h po. für 24-72h oder
- Patiromer 8,4g/24h po.
- Routinemäßge Nutzung von Polystyrolsulfonat (z.B. Resonium®) in der Akuttherapie wird zunehmend kritisch beurteilt
Natrium - Hyponatriämie
Häufige Ursache von Vigilanzminderung oder qualitativer Bewusstseinsstörung in der Notaufnahme, insb. bei Pat. mit Diuretika-Einnahme. Symptomatik sehr individuell, teils erst bei deutlich niedrigen Werten relevante Beschwerden (insb. bei Entwicklung >48h = chronischen Verlauf).
- ≤130mmol/l (wenn nicht vorbekannt)
→ Stationäre Abklärung, Therapie nach Symptomatik - Ab <125mmol/l häufig relevant symptomatisch
Relevant ist notfallmedizinisch vor allem die hypotone Hyponatriämie (hyper-/isotone Hyponatriämien erzeugen kein Hirnödem). Trotz komplexer Diagnostik-Flowcharts sind gerade bei multimorbiden Patient:innen unter Polypharmazie oft mehrere Ursachen denkbar, eine definitiv-klare Abgrenzung der Genese ist in der Notaufnahme häufig nicht sicher möglich.
Hyponatriämie - häufige Ursachen
- Diuretika
- Hypervolämie v.a. Herz- bzw. Leberinsuffizienz
- Übermäßiger (chron.) Bierkonsum („Bierpotomanie“)
- Pseudohyponatriämie bei relevanter Hyperglykämie (pro BZ 100mg/dl / 5,5mmol/l = ca. 2mmol/l Natrium↓)
- Forciertes Trinken von großen Mengen Wasser
Meist langsame Entstehung über Tage/Wochen - dann Korrektur langsam durchführen. In Einzelfällen rasche Entstehung (z.B. forciertes Trinken von literweise Wasser), dann bei relevanter Symptomatik auch rasche(re) Korrektur möglich/sinnvoll.
Symptomatik
- Schwere Symptome: Vigilanzminderung, Koma, Krampfanfall
- Moderate Symptome: Übelkeit, Kopfschmerz, typisch etwas verlangsamt, leicht verwirrt
Akut-Diagnostik
- Labor (jeweils vor Therapie abnehmen sofern vertretbar)
- Serum: Natrium, Osmolalität
- Urin: Natrium, Osmolalität (Natriumspiegel im Urin ist durch Diuretika stark beeinflusst und unter Diuretika-Therapie kaum verwertbar; alternativ kann ev. Urin-Harnstoff bei der Diagnostik weiterhelfen)
- Klinische Einschätzung Volumenstatus
- Weitere Differenzierung nach Flowchart:
Flowchart Hyponatriämie
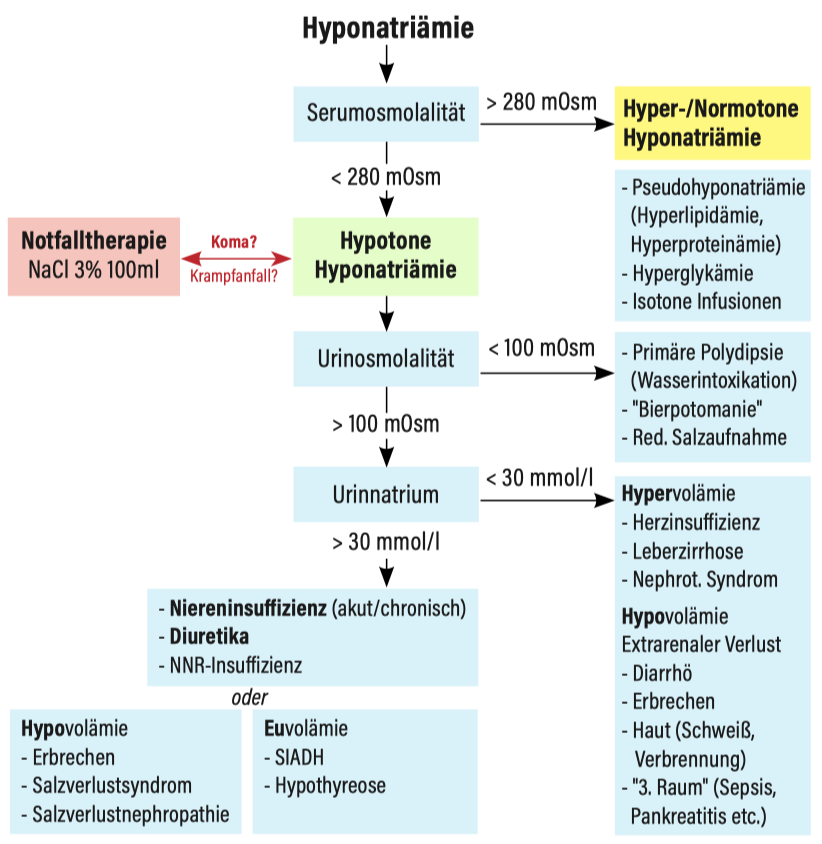
Checkliste Hyponatriämie, Pat. instabil
- Akut-kritische Symptomatik (Krampfanfall, Koma, Hirnödem):
Gabe von NaCl 3% 100-150ml iv. KI über 20 min.- Nach 20min: Kontrolle Natrium-Spiegel (selbe Messmethode wie zuvor), Klinik + bei Bedarf erneute Gabe von NaCl 3% 100-150ml über 20min (max 3x wiederholen)
- Ziel: Besserung der Symptome und Natrium-Anstieg 5 mmol/l
- Intensivmedizinisches Monitoring
- Bei Besserung der Symptomatik hypertones NaCl stoppen, weitere Therapie nach Ursache
- Alternative Ursachen von Vigilanzminderung oder Krampfanfall aktiv evaluieren
Falls NaCl 3% nicht verfügbar
- Falls NaCl 3% nicht verfügbar: Mischen von
- 80ml NaCl 0,9% + 20ml NaCl 10% oder
- 60ml NaCl 0,9% + 40ml NaCl 5,85%
= jeweils 100ml ca. NaCl 3%
- Notfall-Off-Label-Therapie NaBic 8,4% 50ml (in etwa Natriumgehalt von 100ml NaCl 3%), auch periphervenös möglich
Checkliste Hyponatriämie, Pat. stabil
- Ursache eher Hypervolämie (relative Hyponatriämie)
- Häufig reine Wasserrestriktion ausreichend (Trinkmenge 500–700 ml/Tag)
- ggf. vorsichtig Diuretika-Therapie (Furosemid/Torasemid) unter engmaschiger (alle 2h) Natrium-Kontrolle
- Ursache eher Diuretika-induzierte Hyponatriämie
- Pausieren der ursächlichen Medikation - Diuretika
- NaCl-Gabe (0,9%) nur bei Hypovolämie und relevanter (jedoch nicht kritischer, s.o.) Symptomatik!
- Anfangs stündliche Na-Kontrolle
- Berechnung von Na-Bedarf nach Formel (→MDCalc)
- Maximale Korrektur: 10–12 mmol/l in den ersten 24h! Dann 6-8 mmol/l pro 24h
- Bei zu raschem Anstieg: „Gegensteuerung“ mit Glukose 5%-Infusion
Sonderfall "falsche" Hyponatriämie bei Hyperglykämie
Korrigiertes Natrium bei Hyperglykämie (mmol/l)
Natrium (gemessen) → BZ ↓ | 110 | 115 | 120 | 125 | 130 | 135 |
|---|---|---|---|---|---|---|
300mg/dl | 114 | 119 | 124 | 129 | 134 | 139 |
400mg/dl | 116 | 121 | 126 | 131 | 136 | 141 |
500mg/dl | 118 | 123 | 128 | 133 | 138 | 143 |
600mg/dl | 120 | 125 | 130 | 135 | 140 | 145 |
700mg/dl | 122 | 127 | 132 | 137 | 142 | 147 |
800mg/dl | 124 | 129 | 134 | 139 | 144 | 149 |
900mg/dl | 126 | 131 | 136 | 141 | 146 | 151 |
1000mg/dl | 128 | 133 | 138 | 143 | 148 | 153 |
Durch die ausgeprägte Hyperglykämie kommt es zum Flüssigkeits-Shift und Verdünnung des intravasalen Volumens, dadurch entsteht eine Hyponatriämie (diese liegt auch tatsächlich vor und ist kein Messfehler, birgt aber kein Risiko für ein Hirnödem). Bei der Interpretation und der Frage, ob die Hyponatriämie nur durch die Hyperglykämie erklärt werden kann, sollte das „korrigierte“ Natrium beurteilt werden - also der Natriumspiegel, der bei normwertigem Glukosespiegel vorliegen würde.
Berechnung: Pro 100mg/dl (5,6mmol/l) Anstieg der Glucose >100mg/dl ist das korrigierte Natrium um etwa 2mmol/l (je nach Literaturangabe 1,6-2,4mmol/l) höher als das gemessene Serum-Natrium.
Natrium - Hypernatriämie
Deutlich seltener als Hyponatriämie, jedoch hohe Mortalität (insb. ab schwerer Hypernatriämie >160mmol/l).
- ≥150mmol/l: Stationäre Abklärung
Hypernatriämie - Ursachen
Häufigste Ursachen:
- Dehydratation (Wasserverlust ohne Ersatz) z.B. bei vermehrtem Schwitzen, Diarrhö, Erbrechen, Diuretika - oft in Kombination mit
- Verminderte Wasseraufnahme (v.a. bei Hilflosigkeit bei Älteren, Bettlägrigen, Säuglingen)
Seltene Ursachen:
- Diabetes insipidus
- (massiv) vermehrte Natrium-Aufnahme = Salzintoxikation (insb. bei Speisesalz bei Kleinkindern oder Konsum von großen Mengen sehr salzhaltiger Nahrungsmitteln z.B. Sojasauce)
- Iatrogene Natrium-Zufuhr: z.B. hypertone Natrium-Infusionen (inkl. NaBic 8,4%)
Meist langsame Entstehung über Tage/Wochen - dann Korrektur langsam durchführen.
In Einzelfällen rasche Entstehung (z.B. Trinken von großen Mengen Sojasauce oder Konsum von sehr viel Speisesalz), dann bei relevanter Symptomatik auch rasche(re) Korrektur möglich/sinnvoll.
Checkliste Hypernatriämie
- Vorab Berechnung Wasserdefizit (s. unten)
- Hypovolämie/Dehydratation (eher langsam entstanden):
- „Pragmatisches” Therapieschema: Glukose 5% + VEL parallel: Jeweils 1-2ml/kg/h ggf. +Kalium bei Hypokaliämie
- Natrium/(Kalium)-Kontrolle nach 1h, 2h und 4h, Anpassung Infusionsgeschwindigkeit
- Ziel: Max. Reduktion Na 0,5mmol/l pro Stunde, Zielwert Na ≤150mmol/l
- Salzintoxikation/Diabetes Insipidus (akuter Beginn, ausgeprägte Symptomatik):
- Freies Wasser (Glukose 5%) iv., Beginn mit 3(-6)ml/kg/h
- Stündliche Natrium-Kontrolle
- Ziel: Max. Reduktion Na 1mmol/l pro Stunde, Zielwert Na ≤145mmol/l
- Bei zentralem Diabetes Insipidus im Verlauf Desmopressin-Gabe
Berechnung Wasserdefizit
Verschiedene Formeln und Detail-Angaben in der Literatur, jeweils nur grobe Abschätzung möglich:
Variante bei Annahme Natrium-Ziel 140mmol/l:
( (Natriumist / NatriumZiel) -1) x Gesamtkörperwasser = Wasserdefizit (l)
- Gesamtkörperwasser (in Liter):
- ♀: ideales Körpergewicht (kg) x 0,5
- ♂︎: ideales Körpergewicht (kg) x 0,6
→ MdCalc Rechner Wasserdefizit
Alternative, vereinfachte Formel:
4(ml) x Körpergewicht (kg) x Gewünschte Natrium-Korrektur (mmol/l) = Wasserdefizit (ml)
- Beispiel: Bei Natriumist 160mol/l und NatriumZiel 140mmol/l: Gewünschte Korrektur 20mmol/l = 4 x Körpergewicht (kg) x 20
Kalzium - Hypokalzämie
Definition:
- Ionisiertes Ca2+: <1,15mmol/l
- Gesamt-Ca2+: <2,2mmol/l
- bei Azidose verminderte Bindung = mehr ionisiertes Ca2+
- bei Alkalose = vermindertes ionisiertes Ca2+
Ionisiertes / nicht ionisiertes Kalzium - Hintergrund
- ca. 45-50% ionisiertes Ca2+ → nur dieses ist physiologisch aktiv!
- 45% proteingebundenes Ca2+ (80% an Albumin)
- bei Azidose verminderte Bindung = mehr ionisiertes Ca2+
- bei Alkalose = vermindertes ionisiertes Ca2+
- bei Hyperphosphatämie vermindertes ionisiertes Ca2+
Gefahr bei Hypo-/Hyperkalzämie: Rhythmusstörung wegen QTc-Veränderung
Gefahr:
- QTc-Verlängerung (bis zu VT/Torsade de Pointes)
- Krampfanfall
Hypokalzämie - Symptome
- Unruhe, Angst, Nervosität, Müdigkeit
- (Muskel)Schwäche
- Übelkeit, Erbrechen
- Herzrhythmusstörungen
- Chvostek-Zeichen: Klopfen auf N.facialis (1-2cm anterior Ohrläppchen): Zucken Mundwinkel
- Trousseau-Zeichen: Aufpumpen RR-Manschette am Arm über syst. Blutdruck für ca. 3min = Pfötchenstellung (Karpopedalspasmus)
Hypokalzämie - häufige Ursachen + Labordiagnostik
- PTH-Mangel (Hypoparathyreoidismus)
- postoperativ bei Schädigung Nebenschilddrüsen nach Thyroidektomie (häufigste!)
- autoimmun (familiär)
- Hämochromatose/Mb.Wilson, genetische Syndrome, ev. bei HIV
- Hohes PTH (Versuch des Körpers Kalzium zu mobilisieren)
- Vitamin D Mangel (Mangelernährung, Sonnenmangel)
- Chronische Niereninsuffizienz
- Hyperphosphatämie
- erhöhte Gabe und red. Ausscheidung bei akuter / chronischer Niereninsuffizienz
- massiver Gewebeverlust (Rhabdomyolyse oder Tumorlyse)
- Bisphosphonat-Gabe
- Pankreatitis (nekrotisierender Verlauf)
- Funktional bei schwerer Hypomagnesiämie (<0,4mmol/L), selten auch bei massiver Hypermagnesiämie
Labordiagnostik
- BGA
- Kalium, Magnesium
- Nierenwerte
- Diagnostik im Verlauf: Phosphat, intaktes PTH, Albumin, Gesamteiweiß
Checkliste Hypokalzämie - symptomatisch
- Calciumgluconat 10% 30ml iv. KI
- dann ZVK-Anlage + Calciumgluconat 20% 1ml/kg über 12h unter Monitoring
- Bei Hypomagnesiämie: zusätzl. Magnesiumsulfat 10% 40-60ml über 12-24h iv. (ca. 16-24mmol Mg)
Kalzium - Hyperkalzämie
Definition:
- Ionisiertes Ca2+: >1,35mmol/l
- Gesamt-Ca2+: >2,6mmol/l
ionisiertes / nicht ionisiertes Kalzium - Hintergrund
- ca. 45-50% ionisiertes Ca2+ → nur dieses ist physiologisch aktiv!
- 45% proteingebundenes Ca2+ (80% an Albumin)
- bei Azidose verminderte Bindung = mehr ionisiertes Ca2+
- bei Alkalose = vermindertes ionisiertes Ca2+
- bei Hyperphosphatämie vermindertes ionisiertes Ca2+
Gefahr bei Hypo-/Hyperkalzämie: Rhythmusstörung wegen QTc-Veränderung
Gefahr:
- Hyperkalzäme Krise
(Entgleisung meist länger bestehender Hyperkalzämie) - Bradykardie, QTc-Verkürzung
- Rhythmusstörung
Hyperkalzämie - Symptome
- Polydipsie (meist länger vorbestehend, klassisches Symptom)
Weitere Symptome (Auswahl):
- Muskelschwäche
- Akute Niereninsuffizienz, Polyurie
- Übelkeit/Erbrechen
- Pankreatitis
- Verwirrung/Schwäche bis zu Koma
- QTc-Verkürzung (<350ms), Bradykardie, AV-Block
- Hypertension
Hyperkalzämie - häufige Ursachen + Labordiagnostik
- Primärer Hyperparathyreoidismus (PTH) bei Epithelkörperchenadenome
- Osteolyse bei Knochenmetastasen (insb. Mammakarzinom, Myelom)
Labordiagnostik
- BGA
- Kalium, Natrium
- Nierenwerte
- Diagnostik im Verlauf: Phosphat; intaktes PTH; Serum-Elektrophorese, BSG
Checkliste Hyperkalzämie
- Volumengabe
- nur bei Hypervolämie Gabe von Diuretika (kalziumsenkender Akut-Effekt gering) z.B. Furosemid 40mg iv.
- Pausieren von Thiaziddiuretika (HCT, Xipamid)
- Bei Sarkoidose/multiplem Myelom: Dexamethason 40mg/d über 4 Tage
- Bei gleichzeitiger schwerer Nierenfunktionseinschränkung: Dialyse
- Tumorinduzierte Hyperkalzämie:
- Bisphosphonat (z.B. Zoledronat 4mg iv. KI) wenn GFR >35 ml/min.
- Calcitonin 4IE/kg sc. (ca. 200-300IE) alle (6-)12h
- V.a. hyperkalzäme Krise bei Symptomatik + Gesamt-Ca2+ >3,5mmol/l (ionisiertes Ca2+ ca. >2mmol/l)
→ immer Monitorüberwachung!- ggf. auch bei niedrigerem Laborwert, raschem Anstieg + Symptomatik
- Dialyse (z.B. kontinuierliches Verfahren) zur Kalzium-Senkung als Überbrückung erwägen
Blutbild
Anämie / niedriger Hb
Hb und Hkt sind relative Parameter (im Verhältnis zum gesamten Blutvolumen).
Daher CAVE: Bei akuter, massiver Blutung ist Hb (meist) noch „normal“, da Hb-Abfall erst bei „Nachziehen“ von extravasalem Volumen oder Verabreichung von Infusionslösungen (Verdünnung) auftritt.
Anämie - Ursachen und Abklärung:
- Akute („schnelle“) Anämie:
- Blutverlust traumatisch: Intraabdominell, inbes. peritoneal, Becken, Pleuraraum; alternativ Blutverlust "nach außen"
- Blutverlust atraumatisch: GI-Blutung, spontane Blutung insb. (retro)peritoneal, Einblutung in große Muskelgruppen, Hämolyse
- Akut auf chronische Anämie
- Chronische Anämie: Selten für Notaufnahme relevant. Multiple Ursachen, weitere Abklärung im stationären/ambulanten Umfeld.
Therapie/Transfusion nach Klinik und generell zurückhaltend, außer bei V.a. akute vital bedrohliche Blutung (siehe Transfusion).
Einteilung und diagnostisches Vorgehen bei Anämien:
- Verschiedene Einteilungen bei Anämien (z.B. funktionell, Blutbildmerkmale), pragmatisch für Notaufnahme nach MCV und Klinik.
- Weitere hilfreiche Parameter (je nach Verdacht): LDH, indirektes Bilirubin, Haptoglobin (Hämolyse), Retikulozyten bzw. Retikulozytenproduktionsindex (RPI).
- Retikulozytenproduktionsindex gibt Hinweis, ob bei Anämie adäquate Erythropoese („Nachbildung“) stattfindet. Bei niedrigem RPI V.a. Knochenmarkinsuffizienz (z.B. bei hämatologischer Erkrankung wie Leukämie) oder Vitamin B12- oder Folsäure-Mangel. Berechnung → Reticulocyte Index
Mikrozytäre Anämie
- MCV↓, häufig auch hypochrom (MCH↓) = „keine ausreichende Hämoglobin-Bildung“
Anämie mikrozytär - Ursachen
- Eisenmangelanämie bzw. chronische Blutung (Ferritin↓, Transferrin↑, Transferrinsättigung↓)
- Thalassämie (Eisen/Ferritin normal, evtl. Hämolysezeichen)
- Sideroblastische Anämie, Bleivergiftung, chronische Erkrankungen in Spätphase
Anämie mikrozytär - Labordiagnostik
„Eisenstatus“ (ggf. im stationären Verlauf, keine Notfallparameter):
- Transferrin, Transferrinsättigung, ggf. lösl. Transferrin-Rezeptor, ggf. Retikulozyten-Hb
- Ferritin (Ferritin gleichzeitig Akute-Phase-Protein, erhöht bei Entzündung, Stress etc.)
- Serumeisen (Eisen zur alleinigen Einschätzung nicht verlässlich/sinnvoll)
- Suche nach Blutungsquellen insb. GI-Blutung
Vorgehen / Substitution bei Eisenmangelanämie
- Abklärung - Blutungsquellen (Gastrointestinal? Hypermenorrhoe?) oder inadäquate Eisenaufnahme (z.B. bei fleischloser Ernährung)
- Falls Substitution geplant (frühzeitig individuell anpassen):
- Eisendefizit nach Formel berechnen (Hb-Defizit x 200 + 250 = Mangel in Milligramm)
- Primär orale Gabe anstreben: Eisendefizit x 10 = notwendige Menge
- z.B. Eisen 50-100mg jeden 2. Tag po. bis zum Erreichen der berechneten Menge (bei Gabe alle 2 Tage bessere Resporption diskutiert; jedoch auch täglich möglich)
- iv.-Gabe bei schwerstem Mangel, falls mehrere Präparate nicht vertragen sowie bei schwer Kranken (z.B. Dialyse, Tumor-Pat.) erwägen (CAVE: relativ hohes Anaphylaxie-Risiko!)
Normozytäre Anämie
- MCV normal
- V.a. Hämolyse bei LDH ↑, indirektes Bilirubin ↑, Haptoglobin ↓
(Hämolyse ohne Anämie = "kompensierte" Hämolyse - selten)
Anämie normozytär - Ursachen
- Akuter Blutverlust (Retikulozyten↑)
- Hämolyse (LDH↑, indirektes Bilirubin↑, Haptoglobin↓, Retikulozyten↑)
- Chronische Niereninsuffizienz (Retikulozyten↓)
- Sichelzellkrankheit (auch mikrozytär möglich)
- sowie: Tumoranämie, Hypothyreose, G6PD-Mangel, paroxysmale nächtliche Hämoglobinurie (PNH), Aplastische Anämie, Knochenmarksuppression
Anämie normozytär - Labordiagnostik
„Hämolyseparameter“ + im stat. Verlauf evtl. Autoimmun-Antikörper, Blutausstrich:
- Retikulozyten (+Retikulozytenproduktionsindex „RPI“)
- LDH, Haptoglobin, Bilirubin direkt/indirekt
- (im stat. Verlauf ggf. Blutausstrich, direkter Coombs-Test; evtl. Wärme-/ Kälteagglutinine)
- (evtl. auch + Eisenstatus bei V.a. Tumoranämie / Anämie bei chron. Erkrankung)
Makrozytäre Anämie
- (MCV↑), häufig auch normo-/hyperchrom (MCH normal/↑) = „keine ausreichende Zellbildung“
Anämie makrozytär - Ursachen
Ursachen:
- Vitamin B12 Mangel
- Folsäuremangel
- Leberinsuffizienz inkl. chronischer Alkoholabusus
- Myelodysplastische Syndrome, Medikamente (Chemotherapeutika etc.), Typ-A Gastritis etc.
Anämie makrozytär - Labordiagnostik
- Vitamin-B12, Folsäure
- Ggf. Hämolyseparameter, Retikulozyten (s. normozytäre Anämie), Blutausstrich im Verlauf
Sonderfall Sichelzellkrankheit
Sichelzellkrankheit - Hintergrund
Genetisch bedingte Hämoglobinopathie (häufig mit chronischer Anämie), v.a. in östlichem Mittelmeerraum und Afrika verbreitet (Selektionsvorteil hinsichtlich Malaria). Bei Hypoxie verändert sich Form der Erythrozyten, dies führt zu Hyperviskosität.
Folgen: Vaso-Okklusion bis hin zu Infarkten (akute Krise), erhöhtes Infektionsrisiko, Anämie, chronische Organschädigungen
Leitsymptom Schmerz (Okklusion, verminderte Oxygenierung, Infarkt-Reperfusion) bei akuter Krise, teils Ganzkörperschmerz. Sonderform „akutes Thoraxsyndrom“ = neue pulmonale Infiltrate mit Thoraxschmerz, Fieber, Tachypnoe, Bronchospastik, Husten
Sichelzellkrankheit + akute Krise - Vorgehen
- Hydratation (Volumengabe - kristalloide Infusion)
- Analgesie (meist hochdosierte Opioide nötig, z.B. Fentanyl oder Morphin)
- Sauerstoffgabe (bei Hypoxie)
- Prophylaktische Antikoagulation
- Ggf. Transfusion bei Hb <7g/dl (Indikation streng stellen)
Bei akutem Thoraxsyndrom (zusätzlich):
- Stationäre Aufnahme, engmaschige Überwachung
- Breite antibiotische Therapie analog zu Pneumonie, z.B. Ampicllin/Sulbactam 3g iv. + Azithromycin 500mg iv. (s. Antibiotika)
- Hb <7g/dl: Transfusion (bei fulminantem Verlauf ggf. Austauschtransfusion auf Intensivstation nach Rücksprache mit Onkologie)
Thrombozytopenie
Thrombozyten <30.000/µl: Erhöhte Blutungsneigung, spontane Blutungen möglich, CAVE bei Punktionen!
Thrombozytopenie: Blutungsgefahr und Transfusionsindikation
Thrombozytenzahl | Gefahren | Transfusion erwägen bei |
|---|---|---|
<100 | Vermehrte Blutung nach Verletzung (inkl. Venenpunktion) | OP mit sehr hohem Blutungsrisiko |
<50 | Vermehrte Petechien Vermehrte Blutung / Hämatom nach Eingriff | Invasive Intervention (bei Pat. ohne andere Gerinnungshemmung) z.B. ZVK-Anlage, Liquorpunktion, OPs mit hohem Blutungsrisiko, relevanten Blutungszeichen, intrakranieller Blutung |
<30 | Erhöhte Blutungsneigung, spontante Blutung möglich Zusätzliches Risiko bei paralleler Gerinnungstörung und/oder Einnahme von TAH (z.B. ASS), Antikoagulantien | |
<20 | Gelenkpunktion, akute Blutung, zusätzliche Gerinnungsstörung, Fieber, Infekt | |
<10 | Akute Thrombozytopenie (z.B. nach Chemotherapie) |
Checkliste Thrombozytopenie <150.000/µl
Isolierte Thrombozytopenie oder Panzytopenie?
- Großes Blutbild beachten: Vorgehen bei Panzytopenie (s. unten)
- Thrombozytopenie + Anämie: Hämolysezeichen? Verdacht auf TMA (s. unten)
- Pseudothrombozytopenie? (v.a. bei unplausiblen Werten, fehlenden Blutungszeichen)
- Durch Verklumpung im EDTA-Röhrchen auf, Messfehler. Bei Verdacht: Bestimmung aus Heparin/Citrat-Röhrchen anfordern
- Blutungszeichen?
- Suche/Frage nach: Petechien (nicht wegdrückbar), Einblutung Schleimhäute (z.B. Mund, Zungengrund), Zeichen für GI-Blutung, verstärkte Menstruationsblutung
- Gelenkeinblutungen und Hämatome nicht typisch für reine Thrombozytopenie: Hinweis auf (komplexere) Gerinnungsstörung!
- Bedrohliche Ursache möglich?
- TMA (Thrombotische Mikroangiopathie) - TTP, HUS (s. unten)
Thrombozytopenie + Anämie/Hämolyse + evtl. ZNS-Symptomatik + evtl. Niereninsuffizienz - HIT II: Bei Therapie mit Heparin (UFH, NMH)
4T-Test zur Abschätzung (→MDcalc) - DIC (Disseminierte intravasale Koagulopathie):
Gerinnungsstörung, lebensbedrohlich: V.a. bei Sepsis, schwerer Blutung - Agranulozytose:
Verminderte Granulozyten, oft Fieber/ Infekt, Knochenmark-toxische Medikation (inkl. Metamizol) - Schwangere - HELLP: Schwangerschaft + Hämolyse, erhöhte ALT/ AST, Thrombozytopenie
- TMA (Thrombotische Mikroangiopathie) - TTP, HUS (s. unten)
- Andere Ursache (z.B. ITP, VIT, periinfektiös etc.): Bei Blutungszeichen und/oder Thrombozyten <30.000/µl
→ Stationäre Aufnahme, Rücksprache Hämatologie
Thrombotische Mikroangiopathien (TMA)
Überbegriff mehrerer Erkrankungen: Lebensbedrohliche Mikroangiopathien mit thrombotischen Verschlüssen der kleinen Gefäße und folgenden Endorganschäden. Bei Verdacht umgehender Kontakt mit Zentrum-Nephrologie oder innerhäuslicher Nephrologie!
Hinweisend: Unspezifische Allgemeinsymptome (Fieber, AZ-Minderung), ZNS-Symptome (z.B. Krampfanfall, Vigilanzminderung, Verwirrung)
Typisches Labor: Thrombozytopenie + Hämolyse (+ Nierenschädigung insb. bei HUS), Fragmentozyten im manuellen Blutbild (Notfalluntersuchung!)
→ genauere (Verdachts-)Diagnostik bei DD TTP: PLASMIC-Score (→MdCalc) oder siehe unten.
Thrombotisch-thrombozytopene Purpura (TTP): Vermehrte Gerinnungsaktivierung in kleinen Gefäßen durch Depletion (meist autoimmunologisch) von ADAMTS-13. Ausgeprägte Thrombozytopenie, hämolytische Anämie, ggf. Neuro-Ausfälle/Vigilanzminderung, selten schwere Nierenschädigung. In seltenen Fällen auch direkte Endothelschädigung ohne Involvierung von ADAMTS-13 möglich, z.B. medikamenteninduziert insb. bei Immunsupressiva (z.B. Ciclosporin), nach Ganzkörperbestrahlung, Chemotherapie, Transplantation.
Hämolytisch-urämisches Syndrom (HUS): Meist bakterielles Toxin, dass an Endothelzellen bindet (v.a. Nieren) und diese zerstört (Shigatoxin), selten auch durch Medikamente oder bei Schwangerschaft (HELLP, postpartal) ausgelöst. Führt zu Mikrothrombosierung. Primär Nierenversagen, weniger Thrombozytopenie (vgl. TTP), oft blutige Diarrhö. Sonderfall atypisches HUS (aHUS) u.a. bei familiärer Disposition (umstrittener Begriff), meist ohne Diarrhö.
Diagnostik
- Zeitkritische Diagnosestellung, kausale Therapie von TTP via Plasmaseperation
- Frühzeitig Rücksprache mit Nephrologie / nächstem nephrologischen Zentrum
- PLASMIC Score (s.u.) um V.a. TTP zu erhärten: 0-4 Punkte = niedriges Risiko, 5 = intermediäres Risiko, 6-7 Punkte = hohes Risiko, TTP wahrscheinlich
- Blutige Enteritis = V.a. HUS (jedoch nicht beweisend)
- Vor Therapiebeginn Versand an Labor: Test auf ADAMTS13-Aktivität/-Antikörper
Therapie TTP (immer in Rücksprache mit Zentrum / Nephrologie)
- Frühestmögliche Plasmaseperation (Therapie für TTP)
- Falls rasche Plasmaseperation nicht möglich (z.B. weil prolongierte Verlegung in anderes Haus nötig): Nach Rücksprache mit aufnehmenden Zentrum evtl.:
- Ggf. Steroidstoß (Methylprednisolon 1mg/kg bis zu 10mg/kg)
- Ggf. Transfusion von FFP (10-15ml/kg = 2-4 FFP)
- Falls rasche Plasmaseperation nicht möglich (z.B. weil prolongierte Verlegung in anderes Haus nötig): Nach Rücksprache mit aufnehmenden Zentrum evtl.:
- KEINE Thrombozytentransfusion (außer bei lebensbedrohlicher Blutung)
- Steroidstoß
- Bei Nachweis / kritischem Zustand und hochgradigem Verdacht: Antikörper (Rituximab, Caplacizumab)
Therapie HUS: Symptomatisch, ggf. Dialyse. Verlegung in nephrologisches Zentrum.
PLASMIC Score bei V.a. TTP
PLASMIC Score Wahrscheinlichkeit von schwerem ADAMTS13-Mangel 0-4 Punkte: niedriges Risiko | |
|---|---|
Thrombozytenzahl <30.000/µl | 1 Punkt |
Einer (oder mehr) Hämolyse-Zeichen:
| 1 Punkt |
MCV <90 fL | 1 Punkt |
INR <1,5 | 1 Punkt |
Kreatinin <2,0mg/dl | 1 Punkt |
Kein Malignomverdacht | 1 Punkt |
Keine Z.n. Stammzell- oder Organtransplantation | 1 Punkt |
Leukozytose
Definition: Leukozyten >10.000/µl
Neutrophilie
Häufigste Leukozytose. "Linksverschiebung" = vermehrte (>5%) „junge“ (stabkernige) Neutrophile.
Neutrophilie - Ursachen
- Infekt (bakteriell, viral etc.), Entzündung
- Stress, Sport
- Schock
- Glukokortikoide, Katecholamine, (G-CSF)
- Asplenie (+ Milzinfarkt!)
- Zigarettenkonsum (milde Neutrophilie)
- Hyperthyreose, thyreotoxische Krise
- Myokardinfarkt, Vaskulitis
- Myeloproliferative Neoplasien (neben anderen Blutbildveränderungen)
- Chronisch myeloische Leukämie (CML)
- Schwangerschaft
Checkliste Neutrophilie
- Linksverschiebung
- typisch bei Infekt/Entzündung: Infektabklärung, Fokussuche, ggf. Antibiose
- DD CML
- Bei V.a. (neue) hämatologische Erkrankung: Blutausstrich
Akute Leukämie
- Dringender Verdacht bei Leukozyten >100.000/µl (niedrigere/normale Leukozyten aber kein Ausschluss!)
- Blasten im peripheren Blut
- B-Symptomatik (Schwäche, Fieber, Nachtschweiß), Infektneigung
- Auch daran denken bei Bizytopenie: Anämie (normozytär) + Thrombozytopenie (auch ohne signifikante Leukozytose)
Checkliste V.a. Akute Leukämie
- Sofortige hämatologische Vorstellung
- zeitnahe Knochenmarkspunktion
- Zusätzliche Abklärung analog zu Panzytopenie
Andere Leukozytosen
Lymphozytose
- meist reaktiv bei Infekten
- EBV-Mononukleose (typische „Reizformen“)
- Bei V.a. Mononukleose: Schnelltest, EBV-Serologie
Eosinophilie
- Infektion, insb bei Parasiten/Helminthen
- myeloproliferative Erkrankung
- Allergische Reaktion
Basophilie
- Bei Erhöhung parallel zu anderen Leukozyten: Evtl. myeloproliferative Erkrankung
- Normwertig/niedrige Basophile bei sonst erhöhten Leukozyten: Eher reaktive Leukozytose
Monozytose
- Bei mechan. Diff. BB-Zählung werden evtl. Blasten falsch als Monozyten gewertet (kann V.a. Leukämie erhärten, insb. falls manuelle Auswertung dauert)
Leukopenie / Neutropenie
Definition:
- Leukopenie <4000/µl Leukozyten
- Neutropenie <1600/µl Neutrophile
Leukopenie / Neutropenie Ursachen
Verminderte Bildung/Zerstörung/ „Pooling“:
- Bakterielle Infektion / Sepsis
- Virusinfektion (u.a. EBV, HIV, Hepatitis)
- Medikamentenreaktion („allergische Agranulozytose“)
- Mangelernährung (u.a. Vit-B12, Folsäure)
- Zytotoxische Medikamente („zytotoxische Agranulozytose“), insb. Chemotherapeutika
- Splenomegalie („Pooling“)
- Sowie multiple u.a. hämatologische, rheumatologische, autoimmunologische Erkrankungen
Checkliste Leukopenie / Neutropenie
- <500/µl Neutrophile oder <1.000/µl Leukozyten: Meist Umkehrisolation!
Hämatologische Rücksprache, ggf. prophylaktisch kalkulierte Antibiose
- <1.000/µl Neutrophile: Potentiell auslösende Medikamente absetzen, wenn vertretbar
- Bei V.a. Infekt/Fieber:
- Engmaschige Überwachung, potentiell kritische Pat. (Sepsiszeichen?)
- Infektfokussuche, bei Sepsisverdacht raschestmöglich kalkulierte Antibiose
- Labordiagnostik bei unklarer Genese:
- Vitamin B12, Folsäure
- Leberwerte, Hepatitis/HIV/EBV-Serologie
- Blutausstrich
Sonderfall: Medikamentöse Agranulozytose
Symptome (einige Tage bis 3-6 Monate nach Einnahmebeginn):
- Schleimhautnekrosen in Mund/Rachen: Stomatitis, Halsschmerz
- +/- Fieber
- Neutropenie <500/µl; Thrombozyten + Erythrozyten normwertig
- Gefahr: Opportunistische Infektion
Auslösende Medikamente (Auszug):
Metamizol, NSAR, Thiamazol, Carbimazol, Clozapin, Trizyklika, Makrolide, Cephalosporine, Cotrimoxazol, Furosemid, Spironolacton, Thiazide
Therapie:
- Absetzen etwaig auslösender Medikation!
- Umkehrisolation
- ggf. G-CSF nach Rücksprache Hämatologie
- Niederschwellige Antibiotika-Gabe, z.B. Piperacillin/Tazobactam 4,5g iv. /8h.
Panzytopenie / Bizytopenie
Definition:
- Panzytopenie: Leukozyten, Thrombozyten, Erythrozyten jeweils ↓↓ (alle drei Zell-Linien)
- Bizytopenie: Zwei der Zell-Linien ↓↓ (meist selbe Abklärung wie Panzytopenie)
Panzytopenie / Bizytopenie Ursachen
Knochenmarkschädigung/-dysfunktion
- Leukämie, Myelodysplasie, Lymphom
- Anämie + Thrombozytopenie (Bizytopenie) ohne Vitamin B12-/Folsäuremangel: V.a. Leukämie auch ohne Leukozytose
- Miliartuberkulose, Pilzinfektion
- Aplastische Anämie
- Mangelernährung (Vitamin B12, Folsäure)
Zell-Zerstörung
- Disseminierte intravasale Koagulopathie
- TMA/TTP (siehe Thrombozytopenie)
- Hypersplenismus mit Splenomegalie (u.a. Leberzirrhose, Virusinfektion, Malaria, Endokarditis, Rechtsherzinsuffizienz)
Checkliste Panzytopenie / Bizytopenie
Kritische Befunde (immer in Korrelation zu Vor-Werten):
→ zeitnahe Rücksprache Hämatologie!
- Neutrophile Granulozyten <1000/µl (meist Umkehrisolation ab <500/µl)
- Thrombozyten <10.000/µl
- Hb <7g/dl
- Blasten (dann zeitkritischer Blutausstrich!)
Zusätzlich prüfen:
- Splenomegalie?
- Hypokalzämie, Hyperurikämie? (Tumorlysesyndrom?)
- Niereninsuffizienz, LDH-Erhöhung? (TMA, siehe Thrombozyten)
- Vitamin B12 / Folsäure
- Splenomegalie + Lymphadenopathie: Infekt, Autoimmunerkrankung oder Hämatologie (Leukämie, Lymphom)
Niere
In der Notaufnahme wird die Nierenfunktion pragmatisch aus Kreatinin bestimmt (hieraus automatisch berechnet: GFR). Verminderte Urinausscheidung über mehrere Stunden in der Notaufnahme eher unrealistischer Messwert, meist kein reliabler Parameter.
Cave: Gering abfallende GFR wird von Kreatinin nicht erfasst („kreatininblinder Bereich“), erst ab ca. 50% GFR-Verlust. Kreatinin-Bildung ist abhängig von Muskelmasse: Erniedrigtes Kreatinin bzw. verminderter Anstieg z.B. bei verminderter Muskelmasse / chronischer Mangelernährung / Z.n. Extremitäten-Amputation / Bettlägrigkeit / auch bei Schwangerschaft.
Viele Medikamente müssen bei eingeschränkter Nierenfunktion in der Dosis angepasst werden. Hilfreich hierzu: Fachinformation oder Tools wie →Dosing.de (Uniklink Heidelberg)
Nierenfunktionseinschränkung
Häufige Ursachen für Nierenfunktionseinschränkung (Auswahl)
- Prärenal (verminderte Nierenperfusion)
- Volumenmangel (verminderte Flüssigkeitszufuhr, vermehrter Flüssigkeitsverlust (z.B. Diarrhö, wichtig: Diuretika)
- Hypotonie (z.B. Schock, Sepsis etc.)
- Renal (direte Nephronschädigung)
- Tubulusnekrose: Ischämie, Medikamentös (z.B. Zytostatika), selten Kontrastmittel
- Vaskulär: Nierenarterienstenose, Niereninfarkt, Thrombotische Mikroangiopathien
- Infektiös: Pyelonephritis, Urosepsis
- Nephritis
- Postrenal (Harn-Abflussstauung)
- U.a. Nierensteine/Uretersteine, Tumore, Prostatahyperplasie
AKI - Akute Nierenschädigung
Akute Nierenschädigung ("Acute Kidney Injury AKI) - Stadien vereinfacht / pragmatisch für Notaufnahme, nach KDIGO - basierend auf Kreatinin-Wert.
AKI-Stadium | Änderung Kreatinin vs. Vor-Wert (binnen 7 Tagen) | Kreatininwert* bei unbekanntem (aber a.e. normwertigen) Kreatinin-Wert (≤1mg/dl), Näherungswerte |
|---|---|---|
1 | Anstieg 1,5-1,9-fach | etwa 1-2mg/dl |
2 | Anstieg 2-2,9-fach | etwa 2-3mg/dl |
3 | Anstieg ≥3-fach oder Kreatinin ≥4mg/dl oder Anurie ≥12h | |
* Absolute Kreatinin-Werte sind nicht von KDIGO empfohlen (außer für Stadium 3), in der Realität sind oft keine Vorwerte bekannt. Daher in der Tabelle Näherungswerte bezogen auf angenommen normwertiges Vor-Kreatinin.
Azidose (metabolisch, ph <7,2; keine Besserung nach Allgemeinmaßnahmen oder hämodynamisch relevant)
Elektrolytstörung (v.a. Hyperkaliämie; insb. bei Symptomatik (typisch: Bradykardie) ohne Besserung nach Allgemeinmaßnahmen oder bei bereits bekannter schwerer chronischer Niereninsuffizienz)
Intoxikation (mit dialysablem Toxin)
Overload (Volumenüberladung, insb. bei bestehender chronischer/terminaler Niereninsuffizienz, keine Besserung unter Diuretika erwartbar)
Urämie (klinische Symptome: Schwäche/Verwirrung bis hin zu Vigilanzminderung/Koma, Juckreiz, Übelkeit/Erbrechen, Perikarderguss)
Checkliste akute / progrediente Nierenfunktionseinschränkung
- Vor-Werte? Bekannte chronische Nierenerkrankung?
- Metabolische Entgleisung? (Hyperkaliämie, Azidose/Alkalose?)
- Prärenale Genese? (Flüssigkeitsstatus, Medikationsänderungen, Infekt?)
- Postrenale Genese? (Sono zum Ausschluss Harnaufstau obligat)
- Intrarenale Genese? (Urinstatus, Labor; Vielzahl an Ursachen)
Wichtigste intrarenale Ursachen
Ziel: Identifikation kritischer Erkrankungen, z.B.
- Thrombozytopenie + akute Nierenschädigung
→ TMA bedenken! Alternative (häufigere) DD: Infekt/Sepsis - Proteinurie + akute Nierenschädigung, Mikrohämaturie, erhöhte Entzündungszeichen, schnelle Entwicklung (über wenige Tage), Hypertonie, Ödeme u.a. an Augenlidern + Beinen, oft junge Pat. <30J.
→ Nephritisches Syndrom, z.B. RPGN (Rapid Progressive Glomerulonephritis) bedenken: Nephrologie, zeitkritische Behandlung - Infektzeichen + akute Nierenschädigung (erhöhtes CRP/PCT, Leukozytose/Leukopenie, oft Mikrohämaturie)
→ Pyelonephritis/Urosepsis?
CAVE: DD Sepsis mit alternativem Fokus, Niereninsuffizienz als Zeichen der Minderperfusion bei septischem Schock - komplexe Elektrolytstörung + akute Nierenschädigung (Kalium↑ Phosphat↑, Harnsäure↑, LDH↑, Kalzium↓), insb. bei bek. Tumorerkrankung/Lymphom/Leukämie, wenige Tage nach Beginn bis 7 Tage nach Ende Chemotherapie
→ Tumorlyse erwägen. Kontakt Onkologie, Volumen, Therapie Hyperkaliämie, frühzeitig Dialyse
- Allgemeines Vorgehen:
- Ursachen beheben
- prärenal: Nierenperfusion optimieren, z.B. Volumengabe bei Hypovolämie, Blutdruckmedikation bei Hypotonie reduzieren
- postrenal: Mechanisches Abflusshindernis beheben: Katheteranlage bei Harnverhalt bzw. Harnstau, bei „höherem Hindernis“ (Stein, etc.): Urologie
- Dialyseindikation? (AEIOU, s.oben)
- Beendigung/Pausierung nephrotoxischer Medikation (insb. Diuretika, NSAR)
- (Dosis-)Anpassung renal ausgeschiedener Medikation, insb.
- DOAK, niedermolekulares Heparin
- Antibiotika (nach 24-48h Initialtherapie)
- Metformin
- Engmaschige Verlaufskontrolle Elektrolyte (Kalium!) und Kreatinin
- Weitere Diagnostik nach Rücksprache Nephrologie (meist Urinsediment sowie Eiweißdiagnostik im Urin)
- Ursachen beheben
Sonderfälle: Kardiorenales / Hepatorenales Syndrom
Hepatorenales Syndrom
Dekompensierte Leberinsuffizienz führt zu akuter Nierenfunktionseinschränkung (Faktoren u.a.: Vasokonstriktion der Nierengefäße, Aufhebung der renalen Autoregulation, Umverteilung Blutvolumen, verminderte kardiale Leistung, erhöhter intraabdomineller Druck bei Aszites).
- Therapie komplex (stationär via Nephrologie/Gastroenterologie)
- Ausgleich von Hypovolämie
- Gabe von Humanalbumin nach Aszitespunktion
- ggf. Gabe von Vasokonstriktoren (z.B. Terlipressin / Noradrenalin) nach Maßgabe Nephrologie
Kardiorenales Syndrom (Typ 1)
Akute Herzinsuffizienz mit low-output führt über komplexe Kreisläufe zu akuter Nierenfunktionseinschränkung (Faktoren u.a.: renale Minderperfusion, renal-interstitielles Ödem, erhöhter intraabdomineller Druck, venöse Stauung, neurohumorale Gegenregulation, nephrotoxisch Medikation).
- Therapie komplex (stationär via Nephrologie/Kardiologie)
Ziel ist Therapie der Herzinsuffizienz (Optimierung der Hämodynamik)- Behandlung von Rhythmusstörungen / Hypertonie (hier ggf. Vasodilatatoren)
- reduzierte Volumenzufuhr, meist Diuretika - ggf. sequentielle Nephronblockade bei Diuretikaresistenz
Leber
- Transaminasen = Hepatozelluläre Integrität
- GOT (AST = Aspartat-Aminotransferase; Vorkommen in Leber und Muskel)
- GPT (ALT = Alanin-Aminotransferase; Vorkommen in Leber)
- Cholestaseparameter
- GGT (Gamma-Glutamyltransferase)
- AP (Alkalische Phosphatase)
- Parameter für Leberfunktion:
- Gesamteiweiß
- Albumin
- INR (erhöhter INR bei Leberinsuffizienz zeigt nicht automatisch verminderte Gerinnung an; de facto kann auch ein hyperkoagulatorischer Zustand vorliegen!)
- Bilirubin (Erhöhung → Ikterus, s.unten)
- Pankreas / Pankreatitis:
- Lipase (Pankreatitis, ab 3x Normwert)
- bei chronischer Pankreatitis kann Lipase wegen verminderter Bildung trotz akutem Schub im "Normbereich" sein
- Amylase: unspezifischer, nicht hilfreich
- Lipase (Pankreatitis, ab 3x Normwert)
Erhöhte Leberwerte
Erhöhung relevant ab doppeltem Grenzwert. Bei chron. Leberschädigung möglichst Vergleich zu Vor-Werten.
Einteilung:
- Hepatisch: AST/ALT↑
- Cholestatisch: GGT↑ AP↑
- Toxisch: GGT↑↑
Hepatische Leberwerte - Ursachen und Vorgehen
Ursachen:
- Alkoholinduzierte Hepatitis
- NASH (Nichtalkoholische Steatohepatitis) - häufigste Ursache
- Virushepatitis
- M. Wilson
- Autoimmunhepatitis
- Mononukleose (bei Leberbeteiligung)
Vorgehen:
- Medikamentenanamnese (alle Medikamente, inkl. Phytotherapeutika, frei verkäufliches)
- Alkohol-Anamnese
- Sono Abdomen
- Steatosis? Zirrhose? Venöse Stauung? Aszites? Raumforderung/Tumor?
- Hepatitislabor (im stat./ambulanten Verlauf), Suchtest:
- Hep-B Serologie
(HBs-AG, Anti-HBs, Anti-HBc) - Anti-HAV, Anti-HCV, Anti-HDV, Anti-HEV (evtl. + HBe-AG / AntiHBe-AK, HBV-DNA)
- Hep-B Serologie
- weitere Diagnostik im stationären Verlauf
Cholestatische Leberwerte - Vorgehen
Vorgehen = Sono Abdomen:
Obstruktion Gallenwege? (z.B. Choledocholithiasis, Pankreas-Raumforderung)
- Gallenwege dilatiert:
- Steine? Raumforderung Pankreas/Gallengang/Leber?
- → MRCP/ERCP/Endosono (Rücksprache Gastroenterologie)
- Gallenwege nicht dilatiert:
- Klinisch Hinweis auf Cholangitis? (Fieber, Entzündungszeichen + lokaler Druckschmerz)
- sonst weitere Abklärung im stationären Verlauf
Toxische Leberwerte - Vorgehen
Vorgehen:
- Fokus auf Anamnese (Medikation (auch frei verkäufliche!), Nahrungsergänzungsmittel, traditionelle/alternative Medizin/ Tees, Drogen, etc.)
- Pausieren potentiell lebertoxischer Medikation (insb. Antibiotika)
- Abklärung wie Hepatitis / hepatisch (s. oben)
Ikterus
Gelbfärbung der Haut (insb. auch Schleimhäute und Skleren = „gelbe Augen“) durch vermehrtes Bilirubin (>2mg/dl), oft auch mit Juckreiz (Pruritus).
Bilirubin:
- Indirektes Bilirubin: Unkonjugiertes Bilirubin; Abbauprodukt Hämoglobin, zur Leber transportiert, erst dort dann konjugiert
- Direktes Bilirubin: Konjungiertes Bilirubin; von Leber via Gallenblase ausgeschieden
Ikterus - Unterscheidung und Ursachen
Prähepatischer Ikterus: vor allem indirektes (unkonjugiertes) Bilirubin↑
- Hämolyse (siehe Erythrozyten)
- Ineffektive Erythropoese (z.B. Vitamin-B12-Mangel)
Posthepatischer Ikterus: Vor allem direktes (konjungiertes) Bilirubin↑
- Cholestase z.B. Choledocholithiasis, Pankreas-Raumforderung
Intrahepatischer Ikterus: Meist indirektes und direktes Bilirubin↑
- Hepatitis
- Stauungsleber bei (Rechts-)Herzinsuffizienz
- Schockleber (oft massiv erhöhte Transaminasen wegen hypoxischer Leberzellnekrose)
Sonderfälle:
- Mb. Meulengracht: Hereditär, vermindete Enzymaktivität / Konjugation, z.B. nach Stress (Infekt, Trauma), Alkohol, Fasten. Meist nur leichter (Skleren)ikterus ohne sonstig erhöhte Leberparameter, evtl. Schwächegefühl. Keine akute Therapie nötig.
- Dubin-Johnson / Rotor-Syndrom: gestörter Transport des konjugierten Bilirubins aus Leber; keine Akuttherapie nötig, Achtung bei lebertoxischer Medikation.
Hepatitis B
Interpretationshilfe für Hepatitis-B Serologie
Hepatitis B Serologie
HBsAG | Anti-HBs | Anti-HBc | |
|---|---|---|---|
Impfung | - | + | - |
Z.n. Hepatitis B | - | + | + |
Chronische Hep-B | + | +/- | - |
Akute Hep-B | + | - | + |
Nicht geimpft, | - | - | - |
Schilddrüse
- TSH: Thyroidea-stimulierendes Hormon (Feedback via T3/T4), erhöht bei Hypothyreose, vermindert bei Hyperthyreose oder bei zur hoher Substitution.
- T3: Biologisch wirksames Hormon (HWZ ca. 1 Tag)
- T4: Deutlich mehr produziert (in Thyreozyten), wird zu T3 umgewandelt (HWZ ca. 7 Tage)
Hyperthyreose
Definition:
- TSH↓, T3/T4 normal: Latente Hyperthyreose
- TSH↓, T3/T4↑: Manifeste Hyperthyreose
- Kritischer Verlauf: Thyreotoxische Krise
Hyperthyreose - häufige Ursachen
- Immunhyperthyreose (M. Basedow)
- Schilddrüsenautonomie (z.B. Adenom)
- Jodzufuhr (z.B. Amiodaron, jodhaltiges Kontrastmittel) bei Autonomie
- Überdosierung von SD-Hormonen
- Sowie: schnelles Absetzen von Thyreostatika, subakute Thyreoiditis, Gestationsthyreotoxikose
Hyperthyreose + Kontrastmittel-Gabe: Siehe Sonderfall Kontrastmittel bei Hyperthyreose
Sonderform: "Low-T3-Syndrom":
- T3↓, TSH meist normal oder ↓, T4 normal (bei längerer Erkrankung ggf. auch ↓)
- Typisch im Rahmen von Infekten/Sepsis, Myokardinfarkt, Intensivpflichtigkeit
- Keine Akut-Therapie notwendig, jedoch insb. bei T3↓ und T4↓ Marker für schlechte Prognose
Hypothyreose
Definition:
- TSH↑, T3/T4 normal: Latente Hypothyreose:
- TSH↑, T4↓: Primäre Hypothyreose
- Sonderform: TSH↓ (Sekundäre Hypothyreose, Hypophysenvorderlappeninsuffizienz)
- Kritischer Verlauf: Myxödemkoma (dekompensierte Hypothyreose)
Hypothyreose - häufige Ursachen
- Hashimoto-Thyreoiditis (Autoimmunthyreoiditis)
- Z.n. Schilddrüsen-OP, Radiojod-Therapie
- Thyreostatika
- Jodmangel (selten in Mitteleuropa)
Herz
Kardiale Labordiagnostik beschränkt sich im Notfall auf kardiales Troponin und Natriuretische Peptide; Creatinkinase (CK) keine relevante Rolle mehr in der (kardialen) Akutdiagnostik.
Troponin
Troponin Hintergrund
Kardiales Troponin (cTn) existiert nur in kardialer Muskulatur. Diagnostik im Labor: Hochsensitives Troponin-Essay, POCT/Schnelltests je nach Hersteller ggf. auch als „hochsensitiv“ definiert. Unterschiedliche Grenzwerte je nach Hersteller-spezifischem Testverfahren (Assay).
Erhöhtes Troponin (Definition: >99te Perzentile) zeigt myokardiale Verletzung und erhöhtes Mortalitätsrisik - aber nicht immer einen Myokardinfarkt und Notwendigkeit einer Notfall-Koronarangiografie. Daher insb. bei atypischer / nicht vorhandener Klinik nach alternativen Ursachen (s.unten) suchen!
Troponin bei Niereninsuffizienz: Abbau/Ausscheidung von Troponin ist u.a. von der Nierenfunktion abhängig. Bei chronischer Nierenfunktionseinschränkung zeigt ein erhöhter Troponinspiegel nicht immer eine akute myokardiale Ischämie an, zudem besteht bei diesen Pat. nicht selten auch eine chronische myokardiale Verletzung bei chronischer Gefäßerkrankung.
Vorgehen: Individuelle Risiko-Einschätzung nach Klinik, EKG + Troponin (-Verlauf / Delta (▵).
Auch Vor-Werte (Troponinwerte von vorherigen Aufenthalten) können hilfreich zur Einschätzung sein
Troponin-Erhöhung - Ursachen
Myokardiale Ischämie | Keine primäre myokardiale Ischämie | ||
|---|---|---|---|
Typ I klassischer Myokardinfarkt | Typ II O2-Angebot ↓ / | Kardial | Systemisch |
|
|
|
|
Natriuretische Peptide
BNP - Hintergrund
BNP = Früher „Brain natriuretic peptide“, nun „B-type natriuretic peptid“: Synthese und Sekretion primär in Myokard-Zellen. Ausschüttung bei hoher Ventrikelspannung - Spaltung in BNP und NT-proBNP.
Hilfreich u.a. bei V.a. akute Herzinsuffizienz, ggf. auch als Verlaufs-Messwert bei chronischer Herzinsuffizienz (während stationärem Behandlungsverlauf oder als Vergleichswert bei Wiedervorstellung).
Normwerte („Herzinsuffizienz sehr unwahrscheinlich“):
- BNP < 35 pg/ml
- NT-proBNP < 125 pg/ml
Unterschiedliche Grenzwerte nach Labor, multiple Ursachen für Erhöhung (ESC 2021, Auswahl):
BNP-Erhöhung - Ursachen
Kardiale Genese | Nichtkardiale Genese |
|---|---|
|
|
Glukose
(Nüchtern-) Normwert: 60-100mg/dl oder 3,3-5,6mmol/l
„Weiche“ Grenzwerte: Blutglukose ist abhängig von Nahrungsaufnahme.
Unterschiedliche Maßeinheiten (mg/dl vs. mmol/l); s. Tabelle unten
Hypoglykämie
Hypoglykämie - häufige Ursachen
- Insulin
- akzidentiell/suizidal überdosiertes Insulin
- Antidiabetika
- Akkumulation Antidiabetika bei Nierenschädigung
- Nahrungsaufnahme vergessen
- Infekt
- Leberversagen
Definition: <60mg/dl / <3,3mmol/l, bei „typischen“ Symptomen ggf. auch <70mg/dl / 3,9mmol/l
Der genaue BZ-Grenzwert für Hypoglykämie ist international umstritten, liegt meist zwischen 50-70 mg/dl (2,8-3,9mmol/l). Wichtig für die Therapie ist vor allem die klinische Symptomatik.
Therapie der Hypoglykämie siehe schwere Hypoglykämie
Hyperglykämie + Diabetes Mellitus
Definition:
- 100-125mg/dl / 5,6-6,9mmol/l: Gestörte Glukosetoleranz, „Prädiabetes“
- >125mg/dl / >6,9mmol/l (oder nicht-nüchtern >200mg/dl / >11,1mmol/l): V.a. Diabetes mellitus
- >300mg/dl / 16,7mmol/l: IMMER Blutgasanalyse (pH? Elektrolyte?), Ketone? (Urin/Serum)
- → Hinweis auf diabetische Ketoazidose oder hyperosmolare Hyperglykämie?
Serumglukose Umrechnung mg/dl und mmol/l
Serumglukose - Umrechnung | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
mg/dl | 40 | 54 | 60 | 72 | 80 | 90 | 100 | 144 | 200 | 270 | 400 | 540 | 600 | 721 | 800 | 901 | 1000 |
mmol/l | 2,2 | 3 | 3,3 | 4 | 4,4 | 5 | 5,5 | 8 | 11,1 | 15 | 22,2 | 30 | 33,3 | 40 | 44,4 | 50 | 55,5 |
Gerinnung
Das „Gerinnungslabor“ bildet die tatsächliche plasmatische bzw. globale Gerinnung von Patient:innen nur sehr unvollständig ab. Daher sind Blutungszeichen bzw. die hämostaseologische Anamnese wesentlich wichtiger zur Risikostratifizierung und klinischen Einschätzung als isolierte Laborwerte. Gleichzeitig können viele (medikamentös bedingte) Koagulopathien aufgrund einer unauffälligen Labordiagnostik (insb. „Routine“ aus Blutbild, INR/PTT) nicht ausgeschlossen werden.
Mehr zu Blutung und Transfusion siehe Blutung, Gerinnung, Transfusion
INR / PTT
Unauffällige PTT und INR Werte schließen Koagulopathien nicht aus, da sie nur eine sehr geringe Sensitivität und Spezifität bzg. eines erhöhten Blutungsrisikos ausserhalb des Therapiemonitoring von VKA/UFH aufweisen!
INR (Quick)
Da gemessene Quick-Werte unterschiedlicher Labore nicht miteinander verglichen werden können wurde mit der International Normalized Ratio (INR) eine Vereinheitlichung geschaffen (daher nachfolgend INR verwendet). Die INR wurde zur Bestimmung der Wirkung von Vitamin K Antagonisten (VKA) entwickelt. Die INR bildet dabei Faktor VII sowie die gemeinsame Endstrecke der Gerinnung (Faktor X, V, II, I) ab.
Ursachen isolierter INR-Erhöhung:
- Einahme von VKA bzw. Vitamin K Mangel
- Leberinsuffizienz (s. Leberwerte oben)
- Faktor Xa Inhibitoren (z.B. Apixaban/Rivaroxaban)
- DIC
Erhöhung INR unter VKA-Antagonisten - Vorgehen
- INR <10, keine Blutung:
- Pausieren des VKA
- INR Kontrolle am Folgetag
- INR >10, keine Blutung:
- VKA stoppen
- Vit K 2,5-5mg po.
- INR Kontrolle am Folgetag, evtl. orale Vit. K Gabe wiederholen
- (schwere) Blutung:
- VKA stoppen
- Vit. K 10mg iv.
- Substitution von PPSB (1 IE/kg je % Ziel-Quick Differenz iv.)
PTT
"Partielle Thromboplastin Zeit" (PTT) dient zum Monitoring der Therapie mit unfraktioniertem Heparin (UFH), die globale Gerinnung wird wie auch wie durch INR nicht adäquat abgebildet. In der PTT werden die Faktoren XII, XI, IX und VIII abgebildet.
Ursachen isolierter PTT Verlängerung:
- Therapie mit unfraktioniertem Heparin
- Hämophilie A/B, von Willebrand Syndrom (jeweils nur bei schweren Formen)
- Antiphospholipid-Syndrom
- ggf. Therapie mit DOAKs (insb. Dabigatran) oder NMH
- in ca. 15% der Fälle artifizielle Fehlmessung ohne Konsequenz
Verlängerte PTT - Vorgehen
- Keine akute (lebensbedrohliche) Blutung - keine akute Therapie!
- Pausieren von Antikoagulantien erwägen und Verlaufskontrolle nach 6h
- Keine Einnahme von Antikoagulantien? Hämostaseologische Anamnese!
- bei Hinweisen auf Hämophilie weitere hämostaseologische Abklärung (ambulant)
- Lebensbedrohliche Blutung unter UFH
- Antagonisierung mit Protamin (bei unklarer Menge 25mg als Kurzinfusion)
Fibrinogen
Da Fibrinogen der „first Factor down“ im Rahmen einer schweren Blutung ist, sollte eine Bestimmung in der Notaufnahme insb. im Rahmen einer (potentiell) lebensbedrohlichen Blutung erfolgen. Weitere Indikationen zur Bestimmung können der Verdacht auf DIC, Lebersynthesestörung oder V.a. (erworbene) Dysfibrinogenämien sein.
Fibrinogen wird in der Regel durch die "Methode nach Clauss" bestimmt. Während diese Methode im Bereich von 100 bis 400 mg/dl verlässliche Resultate liefert, werden sehr niedrige und sehr hohe Fibrinogenwerte nicht genau erfasst.
Andere Faktoren - Einzelfaktorenbestimmung?
Im Rahmen der Notfalldiagnostik stellt Fibrinogen den einzig sinnvoll zu bestimmenden Faktor dar. Eine weitere Differenzierung von Einzelfaktoren macht im Setting der Notaufnahme nur seltenst Sinn (hohe Kosten, kaum akutmedizinische Relevanz) und sollte nur nach hämosthaseologischer Rücksprache erfolgen.
Ursachen eines erhöhten Fibrinogenspiegels:
- Sepsis/Entzündung (Fibrinogen ist ein Akute-Phase-Protein)
- Therapie mit Kolloiden/Fibrinogenspaltprodukten
Ursachen eines erniedrigten Fibrinogenspiegels:
- Akute Hämorrhagie und Verbrauchskoagulopathie
- CAVE: sehr niedrige/stark abfallende Werte können hinweisend auf eine Hyperfibrinolyse sein!
- Lebersynthesestörung (meist einhergehend mit erhöhtem INR und erniedrigtem Albumin)
- DIC
- Einnahme von DOAKs
Vorgehen - Fibrinogen
- keine akute Blutung - keine akute Therapie
- bei Blutungszeichen Fibrinogen 2-4g iv. als Kurzinfusion substituieren
Im Rahmen des Gerinnungsmanagements sollte eine Fibrinogenspiegelbestimmung immer um eine Thrombelastographie (s. unten) ergänzt werden. Da Fibrinogen ein Akute-Phase-Protein darstellt, ist zudem eine Verlaufsbestimmung von Fibrinogen und Thrombelastographie für das weitere Therapiemanagement sinnvoll.
Anti-Xa-Aktivität
Das Ergebnis der Anti-Xa-Aktivität wird je nach Testkalibierung mit IE/ml oder ng/ml angegeben und sollte physiologisch bei <0,1 IE/ml / <30 ng/ml liegen.
Therapeutisch wird Anti-Xa-Aktivität durch Heparine sowie Xa-Inhibitoren beeinflusst. Je nach eingesetztem Medikament muss die Bestimmung neu kalibriert werden, sodass jeweils mit dem Labor Rücksprache bezüglich der eingesetzten Testmethode und -Kalibrierung gehalten werden sollte.
Durch zunehmend verbreitete Urin-Schnelltests ist der schnelle Ausschluss einer relevanten Antikoagulation durch DOAKs möglich.
Interpretation Anti-Xa-Aktivität
- therapeutische Antikoagulation mit NMH/UFH liegt in der Regel zwischen
0,4-1,0 IE/ml vor- zum Therapiemonitoring Bestimmung 4h nach subcutaner Gabe
- normale Anti-Xa-Aktivität schließt das Vorliegen wirksamer Xa Inhibitor Konzentrationen weitgehend aus z.B. vor Applikation einer Lysetherapie
Thrombelastografie
(z.B. ROTEM®, TEG®)
Thrombelastografie - wichtigste Befunde im Überblick
Hyperfibrinolyse
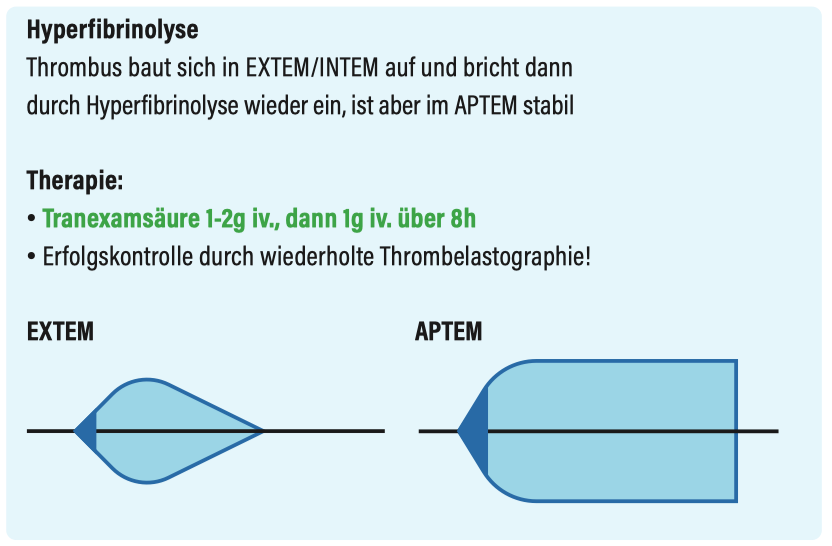
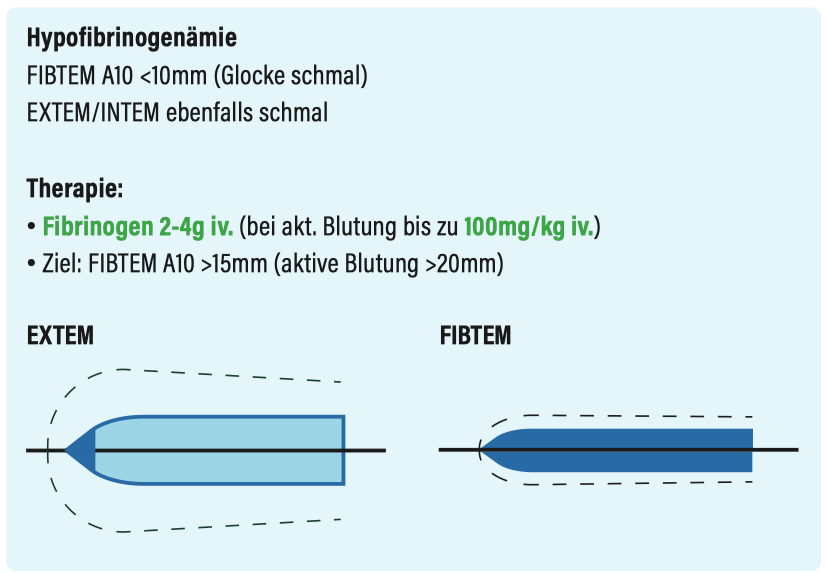
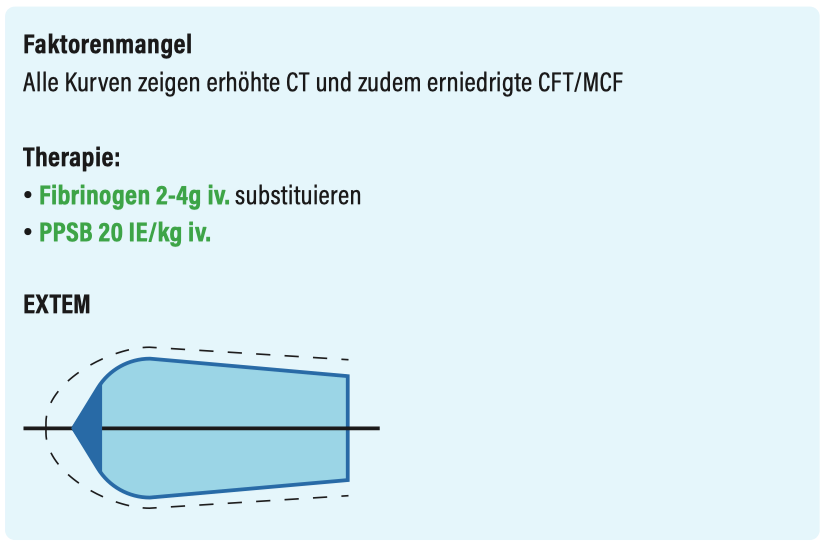
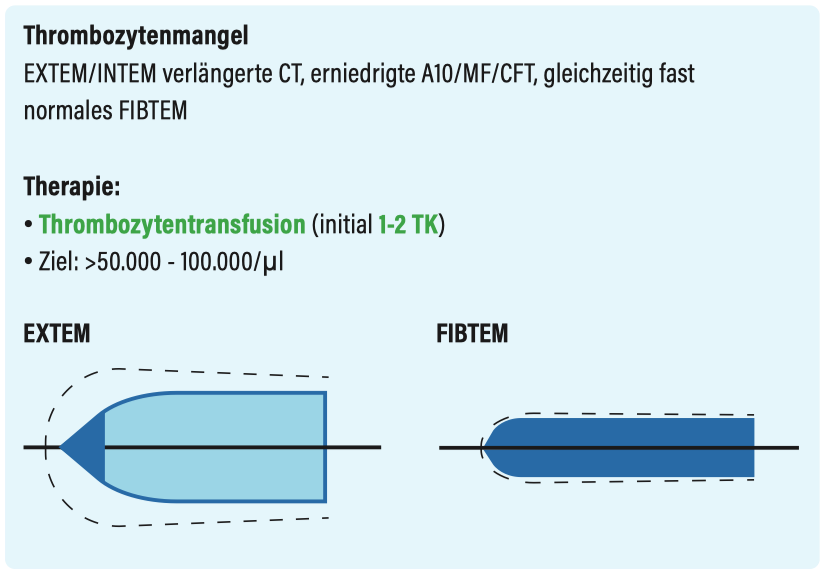
Entzündungszeichen
Wertung von Entzündungsparametern immer in Zusammenschau von Klinik und Gesamtheit der Parameter (inkl. Blutbild: Leukozytose? Linksverschiebung? Leukopenie?). Kein einzelner Parameter kann mit absoluter Sicherheit eine akute bakterielle Infektion beweisen (oder ausschließen).
Antiinfektive Therapie (Antibiose) immer nur bei Kombination aus Labor und Klinik (z.B. spezifischer Fokus, vermuteter Fokus oder Allgemeinsymptomatik bei V.a. Infektion).
PCT vs. CRP: Ein relevanter Vorteil von PCT könnte der frühere Rückgang und damit die Möglichkeit einer früheren Beendigung antibiotischer Therapie sein. Bei Atemwegsinfekten (insb. Bronchitis / Pneumonie / COPD) scheint PCT relativ gut zwischen bakteriellen und nicht-bakteriellen Genesen unterscheiden zu können.
Sinnvolle Nutzung von PCT (jeweils in Zusammenschau mit Klinik)
- Unterscheidung bakterielle / sonstige Exazerbation bei COPD
- Dauer Antibiose (für Notaufnahme nicht primär relevant)
- Detektion zusätzlicher bakterieller Infektion bei anderweitig erhöhtem CRP (z.B. Verbrennungen, Z.n. OP)
- Unterscheidung septische Arthritis und Gichtanfall
CRP vs PCT: Vergleich
CRP | PCT | |
|---|---|---|
Grenzwert | Laborabhängig!
|
|
Erhöht bei |
|
|
Anstieg bei Inflammation | ab ca. 4-6h | ab ca. 2-4h |
Kommentar | Günstiger und vgl. PCT ubiquitär verfügbar, jedoch etwas langsamerer Anstieg (und Abfall), insb. Spezifität für bakterielle Infekte geringer | Sensitiver / spezifischer für bakterielle Infekte als CRP (auch hier keine 100% Sensitivität!). Realer klinischer Vorteil vgl. CRP umstritten. |
Rhabdomyolyse
Muskelzerfall mit Freisetzung von u.a. Kreatinkinase; kann zu Nierenversagen; Flüssigkeits- und Elektrolytstörungen (insb. Hypocalziämie, Hyperkaliämie) führen, selten auch Gerinnungsstörungen (DIC).
Definition:
- Formal ab CK >1000 U/l (unterschiedliche Definitionen)
- Ab 15.000 U/l deutlich erhöhtes Risiko für Komplikationen
Symptome:
- Brauner Urin (Myoglobinurie)
- Muskelschmerz
- Fatigue, Reduzierte Allgemeinzustand, Fieber, Tachykardie
- Nierenversagen (inkl. Azidose, Elektrolytstörung)
Rhabdomyolyse - Ursachen
- Trauma
- Muskelverletzung
- Liegetrauma
- stumpfes Trauma („verprügelt worden“)
- Körperliche Belastung
- Sport (genau fragen!)
- Status Asthmaticus
- Sonstiges
- Intoxikation inkl. Drogen (v.a. MDMA/Amphetamine)
- Infektion
- Medikamente (Statine, Neuroleptika, etc.)
- Myositis
- Hereditär
Checkliste Rhabdomyolyse
- Diagnostik:
- CK: Peak in 24-72hh, langsamer Abfall nach 3-5 Tagen
- <5000 U/l eher geringes Risiko für Nierenversagen, Verlaufskontrolle
- >15.000 U/l erhöhtes Risiko für Komplikationen (= stationäre Aufnahme, Überwachung)
- Myoglobin: Peak schneller, Abfall binnen 1-2 Tage
- CK: Peak in 24-72hh, langsamer Abfall nach 3-5 Tagen
- Therapie: (abseits von Volumengabe keine gute Evidenz für andere Maßnahmen)
- Auslöser beenden (Medikamente prüfen!)
- Volumengabe (Ziel: Diurese 200-300ml/h)
- 3-24l in ersten 24h, dann 500ml/h
- ggf. +Furosemid bei volumenüberladenen Pat. (bei Gefahr von Lungenödem)
- keine generelle „forcierte Diurese" mit Volumen + Diuretika
- ev. Urinalkalisierung (Ziel: ph >6,5); soll Ausfällung von Myoglobin verhindern
- NaBic 150ml 8,4% in 1L G5% über 5h (200ml/h) - über extra Zugang
- NUR wenn: pH <7.5; Serumbikarbonat <30; Kalzium normwertig
- Kontrolle BGA (pH, Kalzium, Bikarbonat) alle 2h - wenn o.g. Werte erreicht NaBic beenden
- Anpassung Infusionsgeschwindigkeit an Urin-pH
- Hypokalzämie NUR korrigieren, falls klinische Symptomatik auftritt (initiale Hypokalzämie bildete sich selbst wieder zurück, Ca-Gabe birgt Risiko der späteren Hyperkalzämie)
- Hyperkaliämie therapieren, ev. Dialyse (bei progred. Nierenversagen) nötig
- enge/frühzeitige Absprache mit Nephrologie
Urinstatus
Der Urinstatus ist eine einfache und billige Methode zur Diagnostik. Allerdings gibt es einige Fehlerquellen der Interpretation, u.a. falsch positive Ergebnisse.
Eine asymptomatische Bakteriurie ist relevant bei Schwangeren und vor urologischen Eingriffen.
Urinstatus - Normalwerte und Ursachen auffälliger Befunde
Normal | Auffällig | |
|---|---|---|
Erythrozyten
| negativ | ↑ bei: Hämaturie typisch bei Infektion, Trauma, Urolithiasis, Malignität, Nephritis ggf. auch ↑ bei Hämolyse, Transfusions-reaktion, Sichelzellkrise, Eklampsie ev. falsch positiv bei Menstruation |
Leukozyten | negativ | ↑ bei: Entzündungsreaktion (z.B. bei Infektion) von Blase, Harnwege, Niere ev. falsch negativ bei Vitamin-C Einnahme, Antibiosen u.a. mit Doxycyclin, Proteinurie, Glukosurie ev. falsch positiv bei STI, Nephritis, ASS-Einnahme, Appendizitis, Kontamination mit Vaginalflüssigkeit, Antibiose u.a. mit Meropenem, Clavulansäure |
Nitrit | negativ | positiv bei: V.a. bakterielle Harnwegsinfektion Cave: Nicht alle Bakterien bilden Nitrit (Pseudomonas, Acinetobacter, Enterococcus) ev. falsch negativ bei Luftexposition, stark verdünnter / saurer Urin, Vitamin ev. falsch positiv bei roten Lebensmittel/Farbstoffe, Kontamination, nicht gekühlte Lagerung, verzögerter Transport |
Ketone | negativ | ↑ bei: Unterernährung/Diät, diabetische Ketoazidose, Eklampsie, Hypothyreose, chron. Alkoholkonsum ev. falsch positiv bei Captopril, L-Dopa |
Protein | negativ | ↑ Nierenerkrankung (glomerulär / tubulär) ggf. auch ↑ bei körperlicher Aktivität / Stress |
pH | 4,5-8,0 | pH↑ u.a. bei Alkalose, lange Zeit zwischen Abnahme und Urintestung, Bikarbonat, ASS-Intoxikation pH↓ u.a. bei Azidose, Diabetes, Unterernährung, Phenylketonurie |
Bakterien | <105/ml | ↑ bei: Bakterieller Infekt (insb. bei Älteren ohne Klinik / DK: Ev. asymptomatische Bakteriurie!) |
Glucose | negativ | ↑ bei: Diabetes Mellitus, (tubuläre) Nierenerkrankung, Schwangerschaft |
Bilirubin | negativ | ↑ bei Ikterus (nur konjugierte Bilirubin) z.B. bei: Lebererkrankung, Cholestase, Pankreatitis/-karzinom |
Urobilinogen | negativ bzw. 0,2-1mg/dl | ↑ bei: Lebererkrankung (Zirrhose, Hepatitis), Hämolyse, Malaria |
Spezifisches Gewicht | 1,010-1,030 g/ml | ↑ bei: Exsikkose, chronischer Herz-/Leberinsuffizienz ↓ bei: Hypervolämie, Diabetes insipidus, Nierenerkrankung, Elektrolytstörung Konstant/unverändert 1,010 g/ml: Zeichen chron. Nierenerkrankung / -insuffizienz |
Spezielle Urin-Analysen
Urinkultur: Einsatz nur bei klarer Indikation, z.B. komplizierter / rezidivierender Harnwegsinfekt, Therapieversagen, schwerer Verlauf, (V.a.) Urosepsis.
Urin-"Toxscreening"
CAVE: Häufige falsch-positive oder falsch-negative Befunde (bis 50%!) bei Urin-Teststreifen.
Kann bei Tagen bis mehreren Wochen zurückliegendem Konsum positiv sein. Viele Substanzen sind nicht nachweisbar - falsch Negative v.a. bei Benzodiazepinen, Opiaten. Daher "Toxscreen" (wenn überhaupt) nur gezielt und als Teil eines Gesamtbildes bei V.a. Intoxikation einsetzen und interpretieren und Limitationen bedenken!
Falsch Positive möglich bei (Auswahl):
- Amphetamine positiv bei Einnahme von
- Metformin
- Promethazin
- Trizyklika positiv bei Einnahme von
- Quetiapin
- Dimenhydrinat
- Carbamazepin
- Benzodiazepine positiv bei Einnahme von
- Sertralin
- sowie bei vorheriger Gabe z.B. durch Rettungsdienst
- Cannabinoide positiv bei Einnahme von
- Ibuprofen, Naproxen
- Opiate (häufig!) positiv bei Einnahme von
- Naloxon
- Quetiapin
- Dimenhydrinat
- Verapamil
- Fluorchinolone
Urin-Natrium / Urin-Osmolalität
Die Anforderung und zeitnahe Untersuchung von Natrium und Osmolalität im Urin kann hilfreich sein, um die Ursache einer unklaren Hyponatriämie einzugrenzen. Die Urinabnahme sollte möglichst vor Gabe von Volumen erfolgen.
Bei dauerhafter Einnahme von Diuretika ist die Aussagekraft von Urin-Natrium gering.
Urin-Sediment
Auch als „Phasenkontrastmikroskopie“ oder „Nephelometrie“ bezeichnet.
Hilfreich bei nephrologischer Diagnostik von unklarer Niereninsuffizienz, Proteinurie im stationären Verlauf.
Auffällig gefärbter Urin
Urin kann aus einer Vielzahl an Gründen auffällig gefärbt sein - nicht alle sind ein Anzeichen für eine akute Pathologie.
Urin-Färbungen und häufige Ursachen
(Auswahl)
- Rote Färbung (meist Hämaturie)
- Infektion (z.B. Zystitis, Pyelonephritis)
- Trauma
- Ureterolithiasis
- Malignität
- akute Nierenerkrankung
- Koagulopathie / Überdosierung Antikoagulanzien
- Hydroxycobalamin (keine Hämaturie, sondern Verfärbung)
- Grüne Färbung
- Propofol
- Amitryptilin
- Methylenblau
- Pseudomonas-Infektion
- Orange Färbung
- Rifampicin
- Porphyrie
- Rot-Braune Färbung
- Myoglobinurie (Rhabdomyolyse)
- Hyperbilirubinämie
- maximal konzentrierter Urin (Hypovolämie, Niereninsuffizienz)
- Lila Färbung
- Bakterien (u.a. Klebsiella pneumoniae, Pseudomonas, E.coli, Enterococcus)
insb. bei länger/dauerhaft einliegendem Katheter auch als "Purple Urine Bag Syndrome" nicht automatisch Zeichen einer akut behandlungsbedürftigen Infektion
- Bakterien (u.a. Klebsiella pneumoniae, Pseudomonas, E.coli, Enterococcus)
Weiterführende Literatur und Links
Interessante Links (frei zugänglich)
- Dosing.de - Dosierung bei Niereinsuffizienz (Uniklinik Heidelberg)
- Treatment of Acute Hyperkalaemia in Adults Clinical Practice Guideline (UK Kidney Association)
- Behandlung der Hyperkaliämie bei Erwachsenen (Arzneimittelkommission BÄK 2023)
- Hypernatremia (StatPearls)
- EKG: Killer-Bs bei Hyperkaliämie (Nerdfallmedizin 2022)
- Leitlinie Eisenmangelanämie (AWMF 2021)
- Nerdfacts Hyperkaliämie (Nerdfallmedizin 2021)
- Akutmanagement der Hyponatriämie (Pin-up-docs 2020)
- Akutmanagement der Hyperkaliämie (Pin-up-docs 2019)
Literatur
- Geldermann, N., Dzimiera, J., Fischer, H. & Christ, M. Acute hyperkalaemia in emergency care: evidence-based approaches. Emerg. Med. J. (2026)
- Jessen, M. K. u. a. Pharmacological interventions for the acute treatment of hyperkalaemia: A systematic review and meta-analysis. Resuscitation 208, 110489 (2025).
- Weismann, D. Symptomatische Hyperkalzämie und hyperkalzämische Krise. J. für Endokrinologie, Diabetol. Stoffwechs. 17, 132–137 (2024).
- Weber, S., Beres, Y., Hossfeld, B. & Kulla, M. Kalzium in der Notfallmedizin — Update 2024. Notfallmedizin up2date 19, 233–249 (2024).
- Lung, C. & Kimmel, M. Nephrologische Notfälle. Notf. Rettungsmedizin 27, 325–335 (2024).
- Stevens, P. E. et al. KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int. 105, S117–S314 (2024).
- Alfonzo, A. et al. Clinical Practice Guidelines Treatment of Acute Hyperkalaemia in Adults. UKKA (UK Kidney Association) (2023).
- Zieschang, M. Behandlung der Hyperkaliämie bei Erwachsenen. Arzneiverordnung in der Praxis 50, 14–29 (2023).
- Sonani, B., Naganathan, S. & Al-Dhahir, M. A. Hypernatremia - StatPearls. (2023).
- Ehmann, M. R. et al. Renal outcomes following intravenous contrast administration in patients with acute kidney injury: a multi-site retrospective propensity-adjusted analysis. Intensiv. Care Med. 49, 205–215 (2023).
- Özcan, F. et al. Thrombotisch-thrombozytopenische Purpura – eine differenzialdiagnostische Herausforderung im Notfall. Med. Klin. - Intensiv. Notfallmedizin 118, 301–308 (2023).
- Carrillo, A. R., Elwood, K., Werth, C., Mitchell, J. & Sarangarm, P. Balanced Crystalloid Versus Normal Saline as Resuscitative Fluid in Diabetic Ketoacidosis. Ann. Pharmacother. 56, 998–1006 (2022).
- Eckardt, K.-U. et al. Nomenklatur für Nierenfunktion und Nierenkrankheiten – Durch Präzision und Verständlichkeit zu besserer Erfassung und Prognose. DMW - Dtsch. Med. Wochenschr. 147, 1398–1406 (2022).
- Walls, R., Hockberger, R., Gausche-Hill, M., Erickson, T. B. & Wilcox, S. R. Rosen’s Emergency Medicine. (2022).
- Loscalzo, J. et al. Harrison’s Principles of Internal Medicine. (2022).
- Herold, G. Innere Medizin 2023. (2022).
- GPOH. S1-Leitlinie Eisenmangelanämie. AWMF (2021).
- Moeckl, T. & Danckwardt, H. Elektrolytstörungen in der Notaufnahme. Notaufnahme up2date 03, 351–362 (2021).
- Emmelheinz, M., Roden, M. & Müssig, K. Endokrinologische Notfälle – Teil 1. Notaufnahme up2date 3, 155–166 (2021).
- Emmelheinz, M., Roden, M. & Müssig, K. Endokrinologische Notfälle – Teil 2. Notaufnahme up2date 3, 227–242 (2021).
- Bednarczuk, T., Brix, T. H., Schima, W., Zettinig, G. & Kahaly, G. J. 2021 European Thyroid Association Guidelines for the Management of Iodine-Based Contrast Media-Induced Thyroid Dysfunction. Eur. Thyroid J. 10, 269–284 (2021).
- Walther, F. Säuren-Basen-Haushalt, Azidosen und Alkalosen verstehen, erkennen und behandeln. (Springer, 2021).
- Mertens, M., Dauben, L., Roden, M. & Müssig, K. Akute diabetische Stoffwechselentgleisungen. Notaufnahme up2date 2, 159–175 (2020).
- Berwanger, U., Conrad, D. & Armbruster, W. Hyperkaliämie in der Präklinik. Notfallmedizin up2date 15, 209–223 (2020).
- Broll, M. & John, S. Hypernatriämie. Med. Klin. - Intensiv. Notfallmedizin 115, 263–274 (2020).
- Rushworth, R. L., Torpy, D. J. & Falhammar, H. Adrenal Crisis. N. Engl. J. Med. 381, 852–861 (2019).
- French, E. K., Donihi, A. C. & Korytkowski, M. T. Diabetic ketoacidosis and hyperosmolar hyperglycemic syndrome: review of acute decompensated diabetes in adult patients. BMJ 365, l1114 (2019).
- Kettritz, R. Hyperkaliämie – Ursachen, Diagnostik und Therapie. DMW - Dtsch. Med. Wochenschr. 144, 180–184 (2019).
- Hernandez, G., Bellomo, R. & Bakker, J. The ten pitfalls of lactate clearance in sepsis. Intensiv. Care Med. 45, 82–85 (2019).
- Bojunga, J. & Mondorf, A. Therapie des Diabetes mellitus bei chronischer Nierenerkrankung. DMW - Dtsch. Med. Wochenschr. 144, 1044–1050 (2019).
- Meyer, G. & Badenhoop, K. Addison-Krise – Risiko erkennen und rasch behandeln. DMW - Dtsch. Med. Wochenschr. 143, 392–396 (2018).
- Harbeck, B. & Lehnert, H. Diagnostik und Therapie der Nebenniereninsuffizienz. DMW - Dtsch. Med. Wochenschr. 143, e177–e177 (2018).
- DGG. S3-Leitlinie Therapie des Typ-1-Diabetes. AWMF (2018).
- Koeppen, M. Störungen des Kaliumhaushalts. AINS - Anästhesiologie Intensiv. Notfallmedizin Schmerzther. 53, 504–514 (2018).
- Müller, M. Störungen des Kalziumhaushalts. AINS - Anästhesiologie Intensiv. Notfallmedizin Schmerzther. 53, 516–528 (2018).
- Milkau, M. & Sayk, F. Thyreotoxische Krise und Myxödemkoma. DMW - Dtsch. Med. Wochenschr. 143, 397–405 (2018).
- Neumeister, B. & Böhm, B. O. Klinikleitfaden Labordiagnostik. (Elsevier, 2018).
- Kasperk, C. Hyperkalzämische Krise und hypokalzämische Tetanie. Internist 58, 1029–1036 (2017).
- Burger-Stritt, S. & Hahner, S. Nebennierenkrise. Internist 58, 1037–1041 (2017).
- Spitzweg, C., Reincke, M. & Gärtner, R. Schilddrüsennotfälle. Internist 58, 1011–1019 (2017).
- Wille, K., Sadjadian, P. & Griesshammer, M. Thrombozytose und Thrombozytopenie – Ursachen und klinische Bedeutung. DMW - Dtsch. Med. Wochenschr. 142, 1732–1743 (2017).
- Zimmermann, H. W., Tacke, F., Kroy, D. & Trautwein, C. Erhöhte Leberwerte – was nun? Dtsch Arztebl 113, A1104–A1108 (2016).
- Meier, J. J. Therapie des Typ-2-Diabetes. Internist 57, 153–165 (2016).
- Spasovski, G. et al. Clinical practice guideline on diagnosis and treatment of hyponatraemia. Eur. J. Endocrinol. 170, G1–G47 (2014).
- Viswanathan, S. Urine Bag as a Modern Day Matula. ISRN Nephrol. 2013, 215690 (2013).
- Overgaard-Steensen, C. & Ring, T. Clinical review: Practical approach to hyponatraemia and hypernatraemia in critically ill patients. Crit. Care 17, 206 (2013).
- Weinbrenner, S. et al. Nationale VersorgungsLeitlinie Chronische Herzinsuffizienz. DMW - Dtsch. Med. Wochenschr. 137, 219–227 (2012).
- Halwachs-Baumann, G. Labormedizin, Klinik - Praxis - Fallbeispiele. (Springer, 2011).