Tipps
- Ohne Versorgung der Blutungsquelle hilft Transfusion und Gerinnungsmanagement nur sehr eingschränkt.
- Daher primär Blutung stoppen! (z.B. mit Packing bei penetrierenden Wunden)
- Der Hämoglobin-Wert bei akut bedrohlicher Blutung ist nicht aussagekräftig (Hb fällt erst im späteren Verlauf ab!)
- Blutprodukte sollen nicht direkt (z.B. über den selben Zugang / Schenkel) mit calciumhaltigen Infusionen gemischt werden (z.B. Ringer-Acetat, Jonosteril®, Sterofundin®), Gefahr von Clotting
Akut lebensbedrohliche Blutung
Bei akut lebensbedrohlicher Blutung: Diagnostik und Therapie parallel, frühzeitig Hilfe zur Blutstillung holen (je nach Quelle, z.B. Endoskopie, Chirurgie…).
CAVE: Bei massiver, akuter Blutung ist Hb-Wert nicht aussagekräftig - nicht auf Abfall warten!
Visuelle Abschätzung von Blutverlust
Oft deutlich erschwert, relevante Über- und Unterschätzung von Blutverlusten. Merkhilfe als Überblick aus der Gynäkologie/Geburtshilfe:
- Blutgesättigte kleine Mullkompresse (10x10cm): 60ml
- Inkontinenzeinlage: 250ml
- Blutgesättigte große Mullkompresse (45x45cm): 350ml
- Blutgefüllte Nierenschale: 500ml
- Postpartale Blutung, auf das Bett beschränkt: 1000ml
- Blutlache auf dem Boden, Durchmesser ca 100cm: 1500ml
- Postpartale Blutung, vom Bett auf den Boden geschwappt: 2000ml
Checkliste Blutung + instabile Patient:in
Basics bei bedrohlichen Blutungen
- Blutung stoppen! (initial keine Zeit mit Labordiagnostik etc. verlieren!)
- Normothermie: Wärmedecke
- Azidose vermeiden: Beatmung anpassen, evtl. NaBic 8,4% 100ml iv. bei pH ≤ 7,2
- Frühe Transfusion: Hb-Zielwert ≥ 9g/dl (≥ 6,6mmol/l
nicht auf Hb-Abfall warten! - Calciumsubstitution: Ziel ≥ 1mmol/l Calcium (ionisiert)
Schock und/oder nicht stillbare / komprimierbare Blutung
- Tranexamsäure 1-2g iv. - blind nur bei schwerem Trauma/V.a. Hyperfibrinolyse
- Fibrinogen 2-4g iv.
- 2 Erythrozytenkonzentrate (bei vitaler Bedrohung auch ungekreuzt 0neg)
- Calcium-Glukonat 10% 20ml iv. KI
- Antikoagulation antagonisieren
Blutabnahme möglichst vor Gabe von Blutprodukten (Bedsidetest MUSS auch bei Notfalltransfusion durchgeführt werden): BGA, Fibrinogen, Blutbild, Quick/PTT, Blutgruppe/Kreuzblut, Thrombelastographie (wenn verfügbar)
Notfall-Gerinnungskarte
Notfall-Gerinnungskarte
In der "Notfall-Gerinnungskarte" von Dr. Casu sind übersichtlich die wichtigsten Schritte bei lebensbedrohlicher Blutung ohne Thrombelastografie (s.u.) aufgeführt.
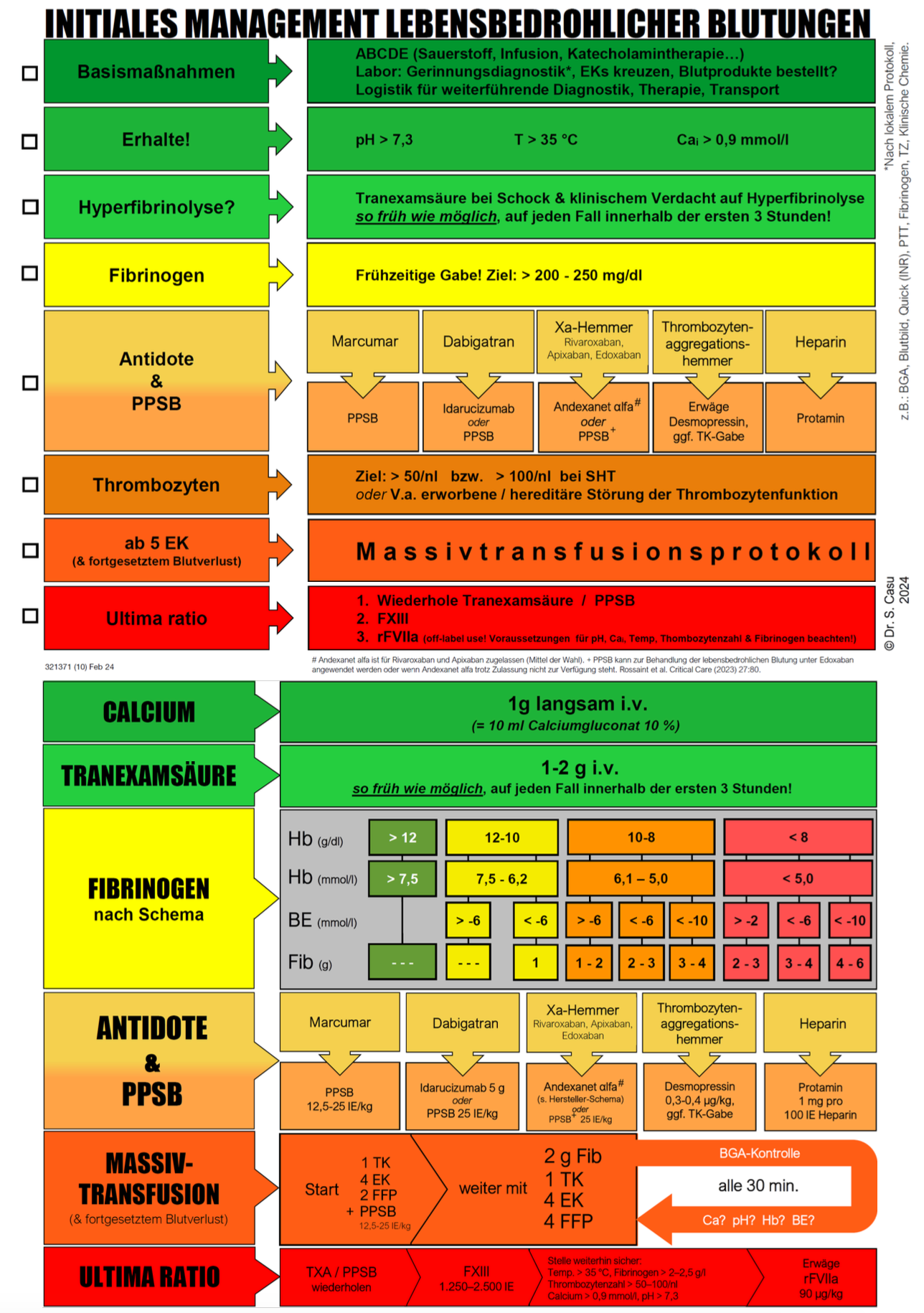
© Sebastian Casu Veröffentlichung mit Genehmigung.
Massivtransfusion
Indikationen
Einzelne Scores können bei der Indikationsstellung helfen. Die Evidenz ist eher eingeschränkt und der klinische Eindruck / Einzelfall sind immer in Betracht zu ziehen!
Trauma: Positiver "ABC-Score" (≥ 2 Punkte)
je ein Punkt für:
- systolischer RR ≤ 90 mmHg
- HF ≥ 120/min
- penetrierendes Trauma
- positive FAST-Sonografie
Allgemein: "Hämorrhagie PLUS 1"
- Kreislaufinstabilität
- Bedarf von ≥ 4 EK in < 1 Stunde oder absehbarer Bedarf > 10 EK in 24h
- Sichtbare, unkontrollierbare Blutung
- starke uterine oder chirurgische Blutung > 1500 ml
- unabhängig von Vitalparametern bei offensichtlicher Exsanguination
Gabe von "Transfusionspaketen" (nach initialem Paket Reevaluation des Bedarf)
1. Paket:
- 4 EKs 0neg
- 2-4 FFPs Blutgruppe AB
- 1 TK
- Tranexamsäure 1-2g iv. (bei Trauma oder nachgewiesener Fibrinolyse, wenn noch nicht erfolgt)
- Fibrinogen 4g iv.
- Calcium-Glukonat 10% 20ml iv. KI
- PPSB nach Thrombelastographie (falls nicht vorhanden 2.000 IE)
jedes weitere Paket:
- 4 EKs (möglichst gekreuzt, sonst 0neg)
- 4 FFPs (entsprechend Blutgruppe des Empfängers, sonst AB)
- 1 TK
- Fibrinogen 2g iv.
OAK + Blutung
Antidota bei lebensbedrohlicher Blutung unter DOAKs + Phenprocoumon
zusätzlich zu allgemeinen Maßnahmen: Wärmeerhalt, Blutstillung, Transfusion
OAK | Antidot | Dosis |
|---|---|---|
| Phenprocoumon (Marcumar®) | PPSB Trockensubstanz zur Auflösung Gabe als KI iv. zusätzlich Vitamin K 10mg iv., dann für 10mg/24h iv. oder po. für 3 Tage | Falls Quick bekannt: PPSB 1 IE/kg erhöht Quick um 1% (Ziel ca. 60-70%) Falls Quick (noch) nicht bekannt / kritische Blutung: PPSB 12,5-25 IE/kg iv. KI |
Apixaban Rivaroxaban | Andexanet alfa Durchstechflasche | Apixaban >5mg / Rivaroxaban >10mg + Einnahme <8h oder nicht bekannt: "hohe Dosis" sonst "niedrige Dosis" |
alternativ: PPSB | PPSB (25-)50IE/kg iv. | |
Dabigatran | Idarucizumab Durchstechflasche | Idarucizumab 5g iv. KI |
alternativ: PPSB | PPSB 25-50IE/kg iv. | |
Edoxaban | PPSB Kein spezifisches Antidot | PPSB 25-50IE/kg iv. |
CAVE: Keine Andexanet-Gabe, wenn zeitnahe Heparinisierung notwendig wird (HLM o.ä.). Heparinwirkung nach Andexanet Alfa Gabe eingeschränkt!
Akute Extremitätenblutung
Das initiale Management unterscheidet sich zwischen polytraumatisierten Patient:innen mit relevanter Extremitätenblutung und bei isolierten Extremitätenverletzungen mit Kreislaufstabilität. Isolierte Blutungen sollten bis zur definitiven Versorgung mit einem Stufenschema abgearbeitet werden.
Isolierte Extremitätenverletzung
Stufenschema / Checkliste
- Hochlagerung der Extremität
- Lokale Kompression (bzw. Kompressionsverband)
- Tourniquet / Blutsperre
Wundinspektion
Bei stark blutenden Wunden sollte bis zur Wundinspektion eine Blutstillung über das Stufenschema erfolgen. Ggf. kann bei starken Blutungen eine Wundinspektion unter Blutsperre/Tourniquet sinnvoll sein. Im Rahmen der Wundinspektion sollte das Material für eine definitive Wundversorgung bereits bereitliegen. Sollte ein primärer Wundverschluss möglich sein und keine relevanten Gefäßverletzungen sichtbar sein, reicht meist eine Wundverschluss zur Blutstillung aus.
Bei Gefäßverletzungen kann je nach Expertise eine Umstechung und Ligatur von kleineren Gefäßästen erfolgen oder eine umgehende chirurgische Vorstellung erfolgen.
Liegen größere Gefäßverletzungen vor, sollte eine manuelle Kompression oder das Setzen von Gefäßklemmen bis zur chirurgischen Versorgung eine Blutstillung erfolgen.
Tourniquet
Insb. bei mehrfachverletzten Patient:innen sollte nach cABCDE / xABCDE eine provisorische Blutstillung stark blutender Extremitätenverletzungen erfolgen. Dies kann initial durch ein proximal der Verletzung angelegtes Tourniquet erreicht werden.
Indikationen:
- Relevante Extremitätenblutung bei Patient:innen mit hämorrhagischem Schock und/oder Polytrauma
- Massenanfall von Verletzten zur initialen Stabilisierung
- Nicht erreichbare Extremitätenblutung, die durch Kompression & Hochlagern oder chirurgische Erstmaßnahmen nicht gestillt werden kann
Checkliste Tourniquet
- Positionierung:
Mindestens 5cm (eine Handbreite) proximal der Verletzung. Keine Anlage an Gelenken, über Wundtaschen/Fremdkörpern oder offenen Frakturen. - Abbinden:
Bereits bei der Positionierung auf enge Bindung der Schlaufen achten. Dann Tourniquet „zudrehen“ bis zum Stillstand der Blutung und distaler Pulslosigkeit. Im Anschluss muss je nach Model der Knebel/Drehverschluss fixiert werden. - Kontrolle:
Distal des Tourniquets muss die Blutung weitgehend sistieren. Ist keine ausreichende Blutstillung möglich, kann die Anlage eines zweiten Tourniquets proximal zum ersten Tourniquet notwendig sein. - Notfall:
Ist die Positionierung direkt proximal der Verletzung (initial) nicht möglich und besteht eine kritische Blutung, gilt: „High and tight“ (proximal an der Extremität anlegen, fest zuziehen!)
Wichtig: Immer die Anlagezeit dokumentieren und übergeben und regelmäßig den korrekten Sitz reevaluieren und ggf. repositionieren! Bei erfolgreicher Stabilisierung der Patient:in steigt oft auch der Blutdruck und damit die Gefahr, dass das Tourniquet nun nicht mehr „fest“ genug sitzt (und dann analog zu einer Venenstaubinde zu einer Verstärkung der Blutung führen kann!).
Tourniquet - Konversion / Abnahme
Sind Patient:innen bereits präklinisch mit einem Tourniquet versorgt worden, sollte eine Konversion/Abnahme des Tourniquets nach initialer Schockraumversorgung erwogen werden. Hierfür sollten Chirurg:in und Material zur Blutstillung bereitstehen und die intiale chirurgische Beurteilung und Versorgung der Wunde unter Tourniquet erfolgt sein.
Cave: Nach Abnahme des Tourniquets kann es zu plötzlichem Kreislaufversagen (erneute Hämorrhagie/Reperfusion) kommen - die Abnahme sollte also im Team kommuniziert und vorbereitet werden!
Ist initial keine chirurgische Wundversorgung möglich, so scheinen Anlagezeiten bis zu 120min möglich zu sein, insgesamt sollte jedoch auf eine möglichst kurze Ischämiezeit und Tourniquetanlage-Dauer geachtet werden.
Transfusion
Transfusionstrigger
Die Indikationen zur Transfusion von Blutprodukten werden in der Querschnittsleitlinie der Bundesärztekammer beschrieben. Zusammenfassend wird ein immer restriktiveres Transfusionsregime empfohlen.
Durchführung: Bedside-Test (auch im Notfall!), Aufklärung, ggf. Sicherungsaufklärung
Transfusionstrigger:
- Erythrozyten:
- Hb < 6g/dl (bzw. <7g/dl bei kritisch Kranken)
- Hb 6-10g/dl und anämiebedingte Symptome (Luftnot, AP, Schwindel) oder Organschaden (Niereninsuffizienz, EKG-Veränderungen etc.)
- Thrombozyten:
- < 10.000/µl
- < 20.000/µl präoperativ (höher, falls potentielle Blutungen nicht komprimierbar sind)
- < 50.000/µl bei Blutungszeichen / aktiver Blutung
- ggf. bei Plättchenhemmung und schwerer Blutung
- Plasmakonzentrate/FFPs:
- Im Rahmen von Massivtransfusionen
- Bei HUS/TTP (therapeutischer Plasmaaustausch)
- Schwache Evidenz zur Gerinnungskorrektur bei Leberinsuffizienz
- Keine Faktorenkonzentrate vorhanden: mind. 30ml/kgKG (Cave Volumenbelastung)
- Substitution von Faktor V und XI (Faktor V nicht als Einzelfaktor vorhanden, Faktor XI als Hämoleven® aus Frankreich oder England beziehbar)
Durchführung Transfusion
- Kreuzblut/Blutgruppe vor Gabe von Blutprodukten abnehmen
- Benötigte Art und Anzahl der Präparate angeben (sowie ggf. bekannte Antikörper), ärztliche Unterschrift auf Anforderungsschein obligat
- Transfusionslabor bestimmt die Blutgruppe und testet auf Antikörper
- EKs werden vorab mittels Kreuzprobe auf Verträglichkeit getestet
- Aufklärung, soweit möglich (s. unten)
- Nach Erhalt der Präparate für Transfusion vorbereiten
- EK nach Lieferung zügig transfundieren (Aufwärmen nur bei Hypothermie oder Massivtransfusion mit geeignetem/zugelassenen Gerät)
- TK unmittelbar nach Lieferung sofort transfundieren
- FFPs vor Transfusion auftauen und sofort transfundieren
- Vorbereiten des Präparates mit geeignetem Transfusionssystem (Filter 170-230µm)
- Entlüften des Infusionssystems
- Bedside-Test durchführen (persönlich am Patientenbett - nicht delegierbar!)
- Patientendaten und Konservendaten inkl. Begleitschein überprüfen
- Bedside Test dokumentieren
- Applikation von ca. 10ml des Blutproduktes, dabei Patient:in bzgl. Transfusionsreaktion beobachten
- Restliche Transfusion über 30-60min verabreichen
- Transfusionsbeutel und -system für 24h bei ca. 4C° lagern und Transfusion in Pat.-Akte dokumentieren
Aufklärung:
Im Notfall ist eine Transfusion auch ohne vorherige Aufklärung möglich, dann aber nachträglich Aufklärung über die verabreichten Präparate und theoretische Risiken! (Ausnahme: Keine Transfusion, wenn Pat. klar und bewusst widerspricht, z.B. Zeugen Jehowas).
Bei stabilen Patient:innen müssen diese oder deren Vorsorgebevollmächtigten IMMER vorab über die Transfusion aufgeklärt werden.
Präparat | Effekt eines Beutels | Besonderheiten |
|---|---|---|
Erythrozyten- EK | Hb steigt | Gabe über 30-60min. Bei Massivtransfusion Aufwärmen mit geeignetem/zugelassenen Bedside Test!! |
Thrombozyten- TK | Thrombozyten steigen | sofort transfundieren - keine Zwischenlagerung Bedside Test nicht verpflichtend |
gefrorenes FFP | 1ml/kg iv. erhöht Gerinnungsfaktoren | Auftauen vor Applikation notwendig, danach sofortige Transfusion Bedside Test! |
Transfusionsreaktion
Bei Verdacht auf einen Transfusionszwischenfall oder ein unerwünschtes Ereignis im Zusammenhang mit einer Transfusion muss Kontakt mit dem Transfusionslabor aufgenommen werden. Transfusionszwischenfälle sowie unerwünschte Ereignisse sind meldepflichtig!
Hämolytische Transfusionsreaktion vom Soforttyp
- Klinik: Schock, Hyperthermie, Hautrötung, Rückenschmerz, Nierenversagen, DIC
- Therapie: Kreislaufstabilisierung, Volumengabe, ggf. Dialyse notwendig, gezielte Gerinnungstherapie
- Diagnostik: Hämolysezeichen? Freies Hämoglobin in Plasma+Urin↑ (alternativ LDH↑, Haptoglobin↓); direkter Coombs Test positiv?
Allergische Transfusionsreaktion
- Therapie und Klinik vergleichbar zu normaler anaphylaktischer Reaktion auf Medikament
- Transfusion stoppen, Adrenalin 0,5mg im., Volumengabe, Prednisolon 1-2mg/kg iv.
TRALI (Transfusion associated Lung Injury)
- Tritt meist akut oder bis zu 6h nach Transfusion von FFPs auf (manchmal auch nach TKs und nur sehr selten EKs)
- Klinik: Akute Dyspnoe, Hypoxie, Lungenödem
- Diagnostik: In Rö-Thorax/CT-Thorax nicht von ARDS zu unterscheiden
- Therapie: NIV / invasive Beatmung, Kreislaufstabilisierung, bereits bei Verdacht Meldung an die zuständige Transfusionsmedizin
TACO (Transfusion associated circulatory overload)
- Tritt meist akut oder bis zu 12h nach Transfusion, typischerweise bei hoher Transfusionsgeschwindigkeit
- Klinik: Akute Dyspnoe, klinisch ähnlich einer akuten kardialen Dekompensation
- Klassisch: Lungenödem. Ggf. gestaute Halsvenen, Hypertension, Tachykardie
- Diagnostik: Klinik, ggf. Sonografie Lunge / Röntgen-Thorax
- Therapie:
- Symptomatisch (z.B. nichtinvasive Beatmung bei Lungenödem)
- Diuretika (z.B. Furosemid) analog zu hypervolämer kardialer Dekompensation
- Transfusionsgeschwindigkeit reduzieren!
Gerinnungstherapie
- Substitution von Gerinnungsfaktoren über FFPs ist seit der Verfügbarkeit von Einzelfaktorenkonzentraten obsolet
- Die Gabe von Gerinnungspräparaten geht mit einem erhöhten thrombogenen Risiko einher
- Bis auf Desmopressin und Tranexamsäure sind alle nachfolgend besprochenen Präparate chargenpflichtig
Tranexamsäure (TXA)
Tranexamsäure ist spätestens seit den CRASH-1 und CRASH-2 Studien ein weit verbreitetes Medikament. Der "reflexartige" Griff zu Tranexamsäure sollte allerdings nach aktueller Evidenz nur noch bei ausgewählten Indikationen erfolgen.
Wirkweise:
- Hemmt die Fibrinolyse durch Hemmung von Plasminogenaktivatoren
- Thrombozytenaktivierende Wirkung wird diskutiert
Indikationen:
- (Schweres) Trauma mit (vermutet) relevanter Gewebsverletzung
- Nachgewiesene Hyperfibrinolyse (mittels Thrombelastometrie)
- Topische Gabe bei Nasenbluten/Zahnfleischbluten etc.
- Inhalation bei pulmonaler Blutung
Dosierung:
- Polytrauma: 1-2g als Bolus sofort (binnen 3h nach Trauma, je früher desto besser) gefolgt von 1g über 8h
- Nachgewiesene Hyperfibrinolyse: 1g als Bolus, weiter nach Thrombelastometrie
- Topisch: Tupfer mit Tranexamsäure auf die Blutung drücken, bei Epistaxis ggf. Verabreichung via Nasalzerstäuber ("MAD®")
- Inhalativ: Tranexamsäure 500mg/5ml über Verneblermaske
Kontraindikationen:
- Relativ: Stillzeit / Schwangerschaft (Risikoabwägung)
Fibrinogen
Fibrinogen wird bei massiver Blutung auch als „First Factor Down“ bezeichnet, da Fibrinogen in den Clot eingebaut und damit verbraucht wird. Insgesamt geht die Gabe von Fibrinogen mit einem verhältnismäßig niedrigem thrombogenen Risiko einher.
Indikation:
- Massive Blutungen
- Nachgewiesener Mangel (Fibrinogenspiegel <100mg/dl bzw. 200mg/dl bei Blutung)
Dosierung:
- 4-6g bei massiver Blutung
- 2g bei Blutung und nachgewiesenem Mangel (weiter nach Spiegel)
PPSB
PPSB vereint alle Vitamin K abhängigen Gerinnungsfaktoren II, VII, IX, X, Protein C und Protein S. Die nicht indizierte Gabe von PPSB geht mit erheblichem thrombogenen Risiko einher.
Indikation:
- Substitution der Gerinnungsfaktoren unter VKA
- Wiederherstellung der Gerinnung unter DOAK
- Substitution von Faktoren bei schwerer Leberinsuffizienz
Dosierung:
- Einnahme von VKA bzw. Leberinsuffizienz:
- Bei bekanntem Quick: IE=kg x (Ziel Quick - aktueller Quick)
- Bei Blutung und unbekanntem Quick: 20-40IE/kg (ca. 2000IE als Kurzinfusion)
- Bei Einnahme von DOAK Gerinnungswiederherstellung durch bis zu 50IE/kg
Cave:
- Die meisten PPSB-Präparate enthalten herstellungsbedingt Heparin, bei bekannter HIT II auf heparinfreies PPSB (z.B. Cofact®) zurückgreifen
Desmopressin
Wirkweise: Freisetzung von vWF und Faktor VIII aus den Weibel-Pallade-Körperchen von Endothelzellen, kurzfristig bessere Aktivierbarkeit von Thrombozyten.
Bereits bei kurzfristig wiederholter Gabe Tachyphylaxie (mehr als 3 Gaben hintereinander nicht sinnvoll).
Indikation:
- Blutung unter
- von Willebrand-Syndrom (ausser Typ 2B)
- Ggf. bei Thrombozytenaggregationshemmern (Wirkung bei ASS+Ticagrelor fraglich)
- Thrombozytopatie (z.B. unter Urämie)
- Therapieversuch bei milder Hämophilie A möglich (wenn kein Faktor VIII Präparat verfügbar)
Dosierung:
- 0,3-0,4µg/kg (maximal 20µg) iv. über 30min
- Wiederholung maximal 2 mal im Abstand von 24h
Nebenwirkungen:
- Hyponatriämie
- Hypotonie bei zu schneller Injektion
- Thrombose (sehr selten)
- Kopfschmerz, Schwindel
Rekombinanter Faktor VIIa (7a)
Der aktivierte Faktor VII gilt als "Kickstarter der Gerinnung", durch die Gabe kann sowohl Hämostase bei unkontrollierbarer Blutung, als auch massive thrombembolische Ereignisse ausgelöst werden. Die Gabe sollte daher nur als Ultima Ratio und wenn möglich nach hämostaseologischer Rücksprache erfolgen.
Indikation:
- Massive, anderweitig nicht kontrollierbare Blutung (Off Label Use)
- Hemmkörperhämophilie
Dosierung:
- 90-120µg/kg
Faktor XIII (13)
Faktor XIII ist essenziell für die Stabilisierung des Fibrinnetzwerks durch Quervernetzung von Fibrinpolymeren. Ein Mangel kann auch bei normwertiger Standardgerinnung zu anhaltender diffuser Blutung führen (z.B. Einstichstellen, Nähte). Die Substitution sollte bei Blutung und nachgewiesener Aktivität < 60 % erfolgen.
Indikation:
- Diffuse Blutung bei normwertiger Standardgerinnung (relative Indikation nach Ausschluss sonstiger Ursachen)
- FXIII-Aktivität < 60 % bei klinischer Blutung
- Angeborener oder sekundärer FXIII-Mangel (Faktor XIII Aktivität <30%)
Dosierung:
- 15–20 IE/kg iv. als Kurzinfusion / über 30min
- Ziel: FXIII-Aktivität > 60 %
Antidote unter DOAK s. Tabelle oben
Thrombelastografie
- Schnell verfügbare (optimalerweise POCT, live beurteilte) Gerinnungsdiagnostik aus Vollblut mit Aussagen zur globalen Gerinnungssituation des Patienten
- Ablesen erster Ergebnisse nach 5-10 Minuten
- 2 Geräte verfügbar (TEG® und ROTEM®), hier wegen größerer Verbreitung in D: ROTEM
- Messung des Widerstands eines Rührstabes in gerinnungsaktiviertem Blut (bei ROTEM als Glocke mit Widerstand in mm abgebildet), Citratblut wird benötigt
- Wiederholung von ROTEM nach jeder Gerinnungskorrektur zur Therapieüberwachung
Messungen
- EXTEM = „Extrinsische Gerinnung“
- Zugabe von Gewebsaktivator (Tissuefaktor) zur Aktivierung der extrinsischen Gerinnung
- INTEM = „Intrinsische Gerinnung“
- Zugabe von Oberflächenaktivator zur Aktivierung (z.B. Ellagsäure) der intrinsischen Gerinnung
- FIBTEM = „Plasmatische Gerinnung“
- EXTEM mit Thrombozyteninaktivierung durch Cytochalasin D
- stellt die plasmatische Gerinnung dar
- APTEM = „Gerinnung ohne Hyperfibrinolyse“
- EXTEM mit Antifibrinolytikum (Aprotinin)
- zeigt die Gerinnung, wie sie ohne Hyperfibrinolyse aussähe (z.B. bei Gabe von TXA)
- HEPTEM = „Gerinnung ohne Heparin“
- INTEM mit Zusatz von Heparinasen
- Zeigt, wie die Gerinnung ohne den Einfluss von Heparin aussähe
Interpretation
- Clotting Time (CT): Zeit von Start bis Clotbildung (INTEM 100-240s / EXTEM 35-80s)
- Alpha Winkel: Anstieg der Clotstabilität
- Clotting Formation Time (CFT): Bildungszeit bis zu einer Festigkeit von 10mm
- A10: Clotstabilität bei 10min (bzw. 20min usw.)
- Maximale Clotstabilität (MCF): maximal erreichte Clotstabilität (Norm 50-75mm)
- Lyseindex (LI): Clotstabilität bei 60min zur MCF in Prozent (Norm <15%)
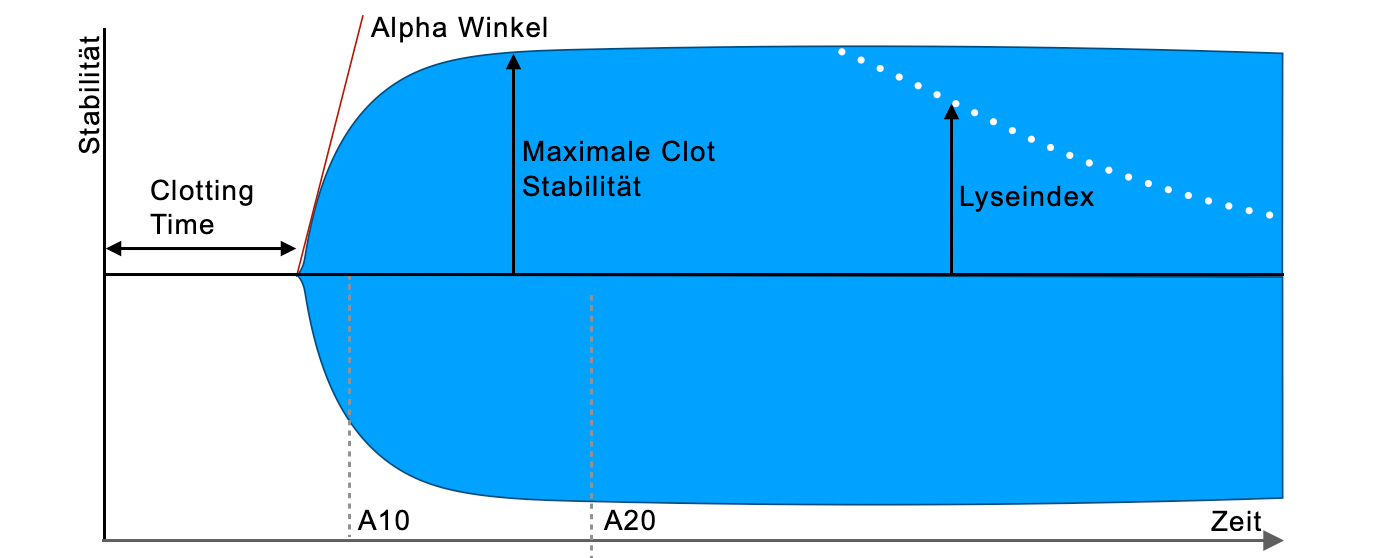
Die abgebildeten Schemata zeigen exemplarisch die relevanten Störungen, die aus der Thrombelastometrie abgeleitet werden können. Thrombelastometrie ist (im Notfall) oft Mustererkennung!
Hyperfibrinolyse
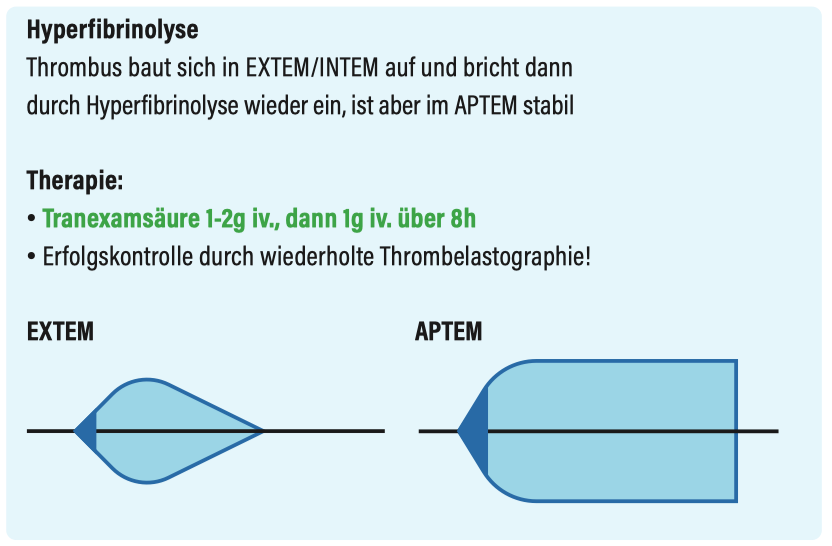
Hypofibrinogenämie
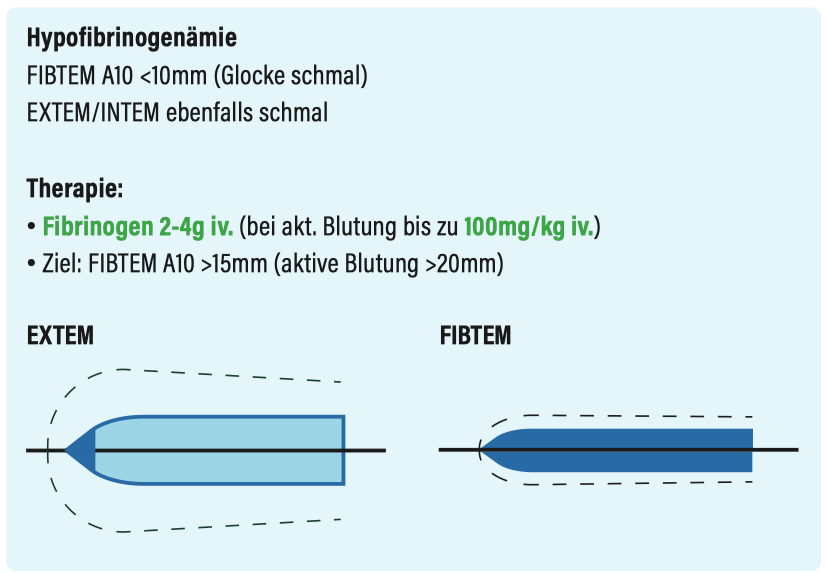
Faktorenmangel
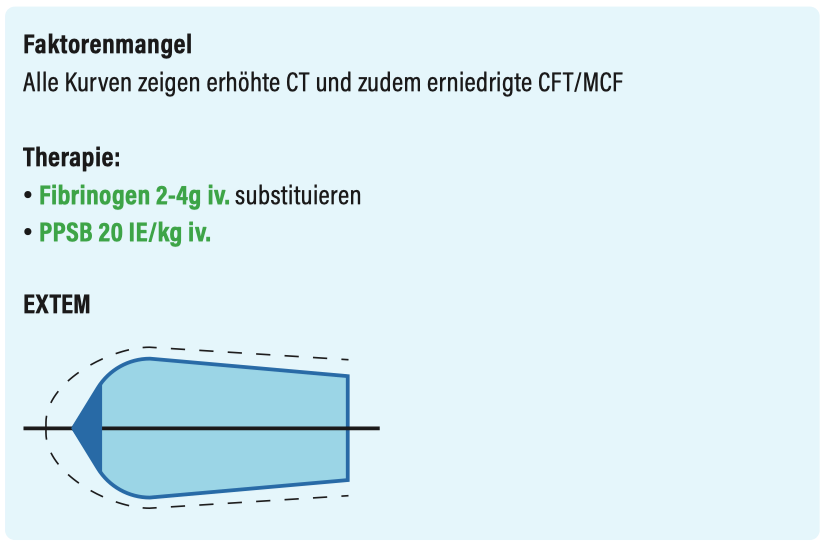
Thrombozytenmangel
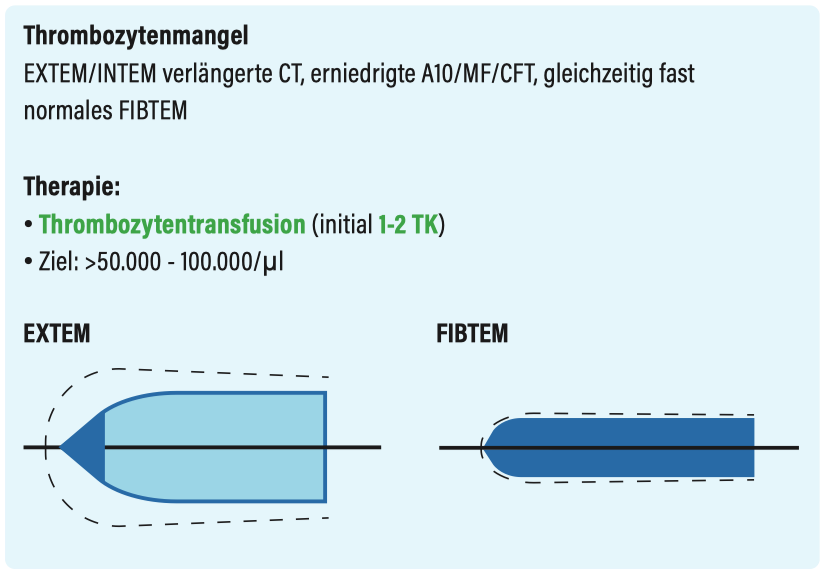
Mehr Informationen zu Antikoagulation siehe auch Antikoagulation.
Häufige Koagulopathien
Iatrogene Thrombozytenfunktionsstörung
Häufigste Ursache für eine Koagulopathie. Viele Medikamente beeinflussen die Thrombozytenfunktion und sollten bei erhöhter Blutungsneigung nur nach Risikoevaluation appliziert werden.
Medikamente, die Thrombozytenfunktion einschränken
- Antibiotika, z.B.
- Ampicillin
- Piperacillin
- Moxifloxacin
- Antiinflammatorische Medikamente, z.B.
- Ibuprofen
- ASS
- Colchicin
- Hydrocortison
- Prednisolon
- Anästhetika, z.B.
- Xylocain
- Kardiovaskulär / Respiratorische Medikation, z.B.
- Theophyllin
- Nitroglycerin
- Verapamil
- Propanolol
- Sonstige, z.B.
- Furosemid
von-Willebrand-Syndrom
Das vWS ist die häufigste angeborene Gerinnungsstörung (symptomatisch ca. 12,5/100.000 Einwohner). Es existieren drei Typen (Typ 1: quantitativer vWF Mangel, Typ 2: qualitativer Defekt von vWF, Typ 3: vollständiges Fehlen von vWF). Gestört ist insb. die Thrombozytenaktivierung, oft zusätzlicher Faktor VIII Mangel.
Diagnostik:
- Im Standardlabor kaum zu erkennen (selten verlängerte PTT)
- Im ROTEM selten verlängerte CFT und ggf. verminderte MCF
Management bei Blutung:
- Lebensgefährliche Blutung: vWF substituieren (Dosis abhängig von Präparat)
- Bei jeder relevanten Blutung (chirurgische/endoskopische Versorgung notwendig)
- Tranexamsäure 1g iv. auch ohne nachgewiesener Hyperfibrinolyse
- Desmopressin 0,3-0,4µg/kg ("1 Amp./ 10kg" da 1 Amp. = 4µg) als iv. Kurzinfusion maximal zweimal wiederholen
Hämophilie A/B
- X-Chromosomal rezessiv vererbbar, 30% Neumutationen (deutlich mehr Männer betroffen)
- Klinisch je nach Ausprägung flächige Blutungen / Gelenkeinblutungen
- Hämophilie A - Mangel an Faktor VIII
- neue Prophylaxe-Therapie: Emicizumab (Hemlibra®)
- Hämophilie B - Mangel an Faktor IX
Diagnostik:
- Verlängerte PTT, meist normale Blutungszeit
- Im ROTEM evtl. verlängerte CT im INTEM
Therapie:
- Leichte Blutung (keine Lebensgefahr, kein drohender Organschaden, gut kontrollierbar)
- Basismaßnahmen (Druckverband, Hochlagern, Wundversorgung)
- Hämophile A ggf. Gabe von Desmopressin 0,3-0,4µg/kg iv KI
- Topische Anwendung von Tranexamsäure
- Schwere Blutung
- Hämophilie A: Faktor VIII Konzentrat 50IE/kg Bolus (weiter nach Faktorenaktivität)
- Hämophilie B: Faktor IX Konzentrat 100-120IE/kg Bolus (weiter nach Faktorenaktivität)
- Wenn nicht verfügbar: FFP (1ml/kg erhöht Faktoren um ca. 0,5-1IE/ml (CAVE: Volumenbelastung)
- Selten: Hemmkörperhämophilie (Alloantikörper oder Autoantikörper) gegen Gerinnungsaktoren, in diesem Fall Gabe von rFVIIa 90 µg/kg alle 2-3h oder ggf. FEIBA 50-100 IE/kg alle 8-12h
- Sonderfall Gelenkeinblutung
- Hämophilie A: Faktor VIII Konzentrat 25IE/kg Bolus
- Hämophilie B: Faktor IX Konzentrat 50 IE/kg Bolus
Bei erwogener Gabe von Faktoren IMMER Rücksprache Hämostaseologie - insb. bei Hemmkörperhämophilie oder bzgl. Materialgewinnung für Plasmaaustauschtest / Bestimmung Bethesda Units.
Disseminierte intravasale Koagulopathie (DIC)
bzw. Verbrauchskoagulopathie. (Globale) Gerinnungsaktivierung führt zu Mikrothromben in der Endstrombahn und Verbrauch von plasmatischen Gerinnungsfaktoren (insb. Fibrinogen) und Thrombozyten. Auslöser sind insb. großflächige Gewebsverletzungen, Infektionen / Sepsis (Meningokokken) oder hämatologische Erkrankungen (insb. AML)
Diagnostik:
- Global kompromittierte Gerinnung (hoher INR/PTT)
- Abfall von Fibrinogen / Thrombozyten (sowie Antithrombin III)
- Teils massiv erhöhte D-Dimere (unauffällige D-Dimere schließen DIC aus)
Therapie:
- Faktorensubstitution (insb. Fibrinogen) sowie ggf. Thrombozytentransfusion
- Bei milder DIC ohne Blutungskomplikationen ggf. prophylaktische Heparingabe
Der ISTH (International Society of Thrombosis & Hemostasis) DIC Score hilft bei der Evaluation bzgl. des Vorliegens einer DIC:
- ≥ 5 Punkte: DIC ist bei passender Klinik hoch wahrscheinlich
- < 5 Punkte: DIC unwahrscheinlich (DD chronische DIC, ggf. Tests engmaschig wiederholen!)
Test / Labor | 0 Punkte | 1 Punkt | 2 Punkte | 3 Punkte |
|---|---|---|---|---|
INR | INR <1,3 | INR 1,3-1,7 | INR >1,7 | |
Fibrinogen | >100 mg/dl | <100 mg/dl | ||
D-Dimere | <400 ng/ml | 400-4000 ng/ml | >4000 ng/ml | |
Thrombozyten | >100.000 /µl | 50.000-100.000 /µl | <50.000 /µl |
Weiterführende Literatur und Links
Interessante Links (frei zugänglich)
- Gerinnungssimulator für viskoelastische Verfahren (VHA-Simulator)
- Europäische Leitlinie massive Blutung und Koagulopathie nach Trauma 6. Edition (2023)
- Gerinnung verstehen (Nerdfallmedizin 2019)
- Gerinnungstherapie im Notfall (Nerdfallmedizin 2019)
- Artikel zur Gerinnung und Gerinnungstherapie (Pin-up-Docs)
Literatur
- Biller-Friedmann, K. & Bayerlein, J. Visuelles Abschätzen von Blutverlusten. Die Anaesthesiol. 74, 384–394 (2025).
- Goldin, M., Tsaftaridis, N., Jnani, J. & Spyropoulos, A. C. Reversal of Direct Oral Anticoagulants (DOACs) for Critical Bleeding or Urgent Procedures. J. Clin. Med. 14, 1013 (2025).
- Schmitt, F. C. F. et al. Update der Point-of-care-basierten Gerinnungstherapie. Die Anaesthesiol. 73, 110–123 (2024).
- Rossaint, R. et al. The European guideline on management of major bleeding and coagulopathy following trauma: sixth edition. Crit. Care 27, 80 (2023).
- Lier, H., Gooßen, K. & Trentzsch, H. Die Kapitel „Stop the Bleed – Prähospital“ sowie „Gerinnungsmanagement und Volumentherapie (Schockraum)“ in der neuen S3-Leitlinie „Polytrauma/Schwerverletzten-Behandlung“. Notf. Rettungsmedizin 26, 259–268 (2023).
- Schell, M., Nägele, F. L. & Thomalla, G. Antikoagulation antagonisieren bei intrakranieller Blutung – Schritt für Schritt. Neurol. up2date 06, 112–118 (2023).
- Metze, M., Platz, M., Pfrepper, C. & Petros, S. Gerinnungsdiagnostik im klinischen Alltag – Teil 2. Die Inn. Med. 63, 736–750 (2022).
- Metze, M., Platz, M., Pfrepper, C. & Petros, S. Gerinnungsdiagnostik im klinischen Alltag – Teil 1. Die Inn. Med. 63, 619–630 (2022).
- Treml, B., Hochhold, C., Fries, D. & Ströhle, M. Gerinnungswirksame Medikamente im Notfall. Notf. Rettungsmedizin 24, 166–172 (2021).
- Hilbert-Carius, P., Wrigge, H. & Koch, R. Einfach und praktisch: Gerinnungsmanagement beim Trauma ohne viskoelastische Testverfahren. Notf. Rettungsmedizin 24, 242–247 (2021).
- Lorenz, B. Einfach und praktisch: Thrombelastographie. Notf. Rettungsmedizin 23, 218–224 (2020).
- Lier, H. & Michael, M. Notaufnahme: Management starker Blutungen. Notaufnahme up2date 1, 47–63 (2019).